
【题目】某温度下,在容积不变的密闭容器中进行如下反应:2X(g)+Y(g)![]() Z(g)+W(s)(正反应为吸热反应),反应一段时间后达到平衡状态。下列叙述正确的是
Z(g)+W(s)(正反应为吸热反应),反应一段时间后达到平衡状态。下列叙述正确的是
A. 加入少量W,逆反应速率增大
B. 通入一定量氦气,压强增大,平衡向正反应方向移动
C. 升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
D. 降低温度,正反应速率减小,逆反应速率减小,平衡向逆反应方向移动
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)1.01×105Pa、0℃时气态单质Xn的密度为d g/L,则X的相对原子质量为________。
(2)NO和O2可发生反应:2NO+O2=2NO2,现有amolNO和bmolO2充分反应后氮原子与氧原子的个数比为_____。
(3)已知铝的相对原子质量为27,若阿伏加德罗常数取6.02×1023mol-1,则可估算一个铝原子的质量约为________g。
(4)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,那么c g氧气在标准状况下的体积约是______(用含NA的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富马酸亚铁(C4H2O4Fe)常用于治疗缺铁性贫血,也可作食品营养强化剂,它可由糠醛(![]() )和硫酸亚铁制备。已知
)和硫酸亚铁制备。已知![]() 。
。
回答下列问题
I.制备富马酸(实验装置如图所示,夹持装置已略去)

(1)将45.0g氯酸钠、0.2g五氧化二钒置于三颈烧瓶中,加入适量水,滴加糠醛并加热至90~100℃,维持此温度3~4h。实验中冷凝管的作用是_________,冷却液宜从___________ (填a”或“b”)处进入。
(2)冰水冷却使其结晶,并通过___________操作可以得到富马酸粗品。
(3)再用1mol·L-1HCl溶液重结晶,得到纯富马酸。该操作中用1mol·L-1HCl溶液的原因是_____________。
Ⅱ.合成富马酸亚铁
(4)取富马酸溶于适量水中,加入碳酸钠并加热、搅拌,调节pH6.5~6.7,产生大量气泡。写出该反应的化学方程式:___________。
(5)将硫酸亚铁溶液和适量的Na2SO3溶液缓慢加入上述反应液中,维持温度100℃并充分搅拌3~4h。
①该操作过程中加入适量的Na2SO3溶液,其目的是___________。
②写出生成富马酸亚铁的离子方程式:_____________。
(6)过滤、干燥得到产品。
过滤时滤纸要紧贴漏斗内壁,原因是________。
Ⅲ.产品纯度测定
(7)取0.300g样品置于250mL锥形瓶中,加入15.00mL硫酸,加热溶解后冷却,再加入50.00mL新沸过的冷水和2滴邻二氮菲指示液,此时溶液呈红色;立即用0.1000mol·L-1硫酸铈(Ⅳ)铵[(NH4)2Ce(SO4)3]标准液滴定(还原产物为Ce3+),滴定终点溶液变为浅蓝色。平行测定三次,平均消耗17.30mL标准液,则样品的纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 离子化合物一定是由金属与非金属元素组成的
B. 离子化合物中可能含有离子键
C. 离子化合物中一定只含有离子键
D. 离子化合物中可能不含有金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
诺氟沙星为喹诺酮类抗生素,其合成路线如下:
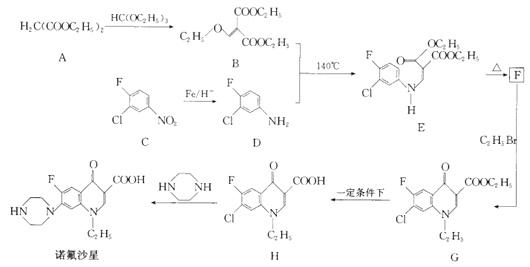
回答下列问题:
(1)化合物A的名称是____________。
(2)诺氟沙星分子中含氧官能团的名称为____________。
(3)C生成D,H生成诺氟沙星的反应类型分别是___________、___________。
(4)F的结构简式为_______________。
(5)G生成H的化学方程式为__________________。
(6)有机物X比B分子少一个CH2原子团,且含有酯基和![]() 结构其中核磁共振氢谱有三组峰,峰面积比为1:3:3的结构简式为__________(任写一种)
结构其中核磁共振氢谱有三组峰,峰面积比为1:3:3的结构简式为__________(任写一种)
(7)参照上述合成路线写出由有机物![]() 、B为有机原料合成
、B为有机原料合成 的路线图______________(无机试剂任选)。
的路线图______________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)![]() CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )
CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是 ( )

A. 该反应的ΔH=+91 kJ·mol-1
B. 加入催化剂,该反应的ΔH变小
C. 反应物的总能量小于生成物的总能量
D. 如果该反应生成液态CH3OH,则ΔH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题。
(1)砷的基态原子的电子排布式为___________________。
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为______________。
(3)NH3的沸点比PH3高,原因是___________;PO43-离子的立体构型为___________。
(4)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为______________。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3 酸性强的原因_____________________。
(6)磷的一种单质白磷(P4)属于分子晶体,其晶胞结构如下图。已知最近两个白磷分子间的距离为 a pm(1pm=10-12m),阿伏加德罗常数的值为NA,则该晶体的密度为__________________g/cm3(只要求列算式,不必计算)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com