
进行下列实验操作时,一般情况下不应该相互接触的是
A.用移液管移取10 mL NaOH溶液并放于锥形瓶中,移液管的尖嘴和锥形瓶的内壁
B.减压过滤时,布氏漏斗下端管口与吸滤瓶的内壁
C.实验室将HCl气体溶于水时,倒扣的三角漏斗口与烧杯内的水面
D.分液操作分出下层液体时,分液漏斗下端管口和烧杯的内壁
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数的值.下列叙述正确的组合是( )
①14g乙烯和丙烯的混合物中氢原子数为2NA个
②0.1mol•L﹣1的FeCl3溶液滴入沸水形成的胶体粒子的数目为0.1NA个
③标准状况下,2.24L Cl2通入足量的NaOH溶液中转移的电子数为0.1NA个
④25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH﹣ 数目为0.2NA个
⑤常温下,100mL 1mol•L﹣1Na2CO3溶液中阴离子总数大于0.1NA个
⑥1mol Na2O2与足量水蒸气反应转移电子数为NA个
⑦常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA个.
A.①④⑤⑦ B. ②⑤⑥⑦ C. ①③⑤⑥ D. ①③⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,
反应的化学方程式如下:2NH3(g)+CO2(g)  NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0
(1)如用右图装置制取氨气,你所选择的试剂是 。

(2)制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。
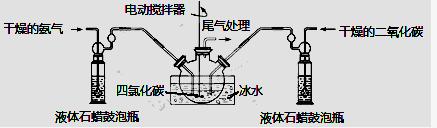
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是: 、 。液体石蜡鼓泡瓶的作用是: 。
②从反应后的混合物中分离出产品,为了得到干燥产品,应采取的方法是_______ (填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
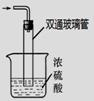
③尾气处理装置如右图所示。双通玻璃管的作用: ;
浓硫酸的作用: 、 。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品11.73 g,用足量石灰水 充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为15.00 g。则样品中氨基甲酸铵的物质的量分数为 。
[Mr(NH2COONH4)=78g/mol、Mr(NH4HCO3) =79 g/mol、Mr(CaCO3)=100 g/mol]【来.源:全,】
查看答案和解析>>
科目:高中化学 来源: 题型:
利用下列实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤作用的活性物质。
下列说法错误的是( )
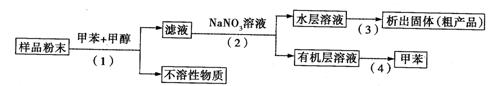
A.步骤(1)需要过滤装置 B.步骤(3)需要用到蒸发皿
C.步骤(4)是利用物质的沸点差异进行分离的
D.活性物质易溶于有机溶剂,难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列鉴别方法不可行的是
A.用水鉴别乙醇、甲苯和溴苯
B.用酸性高锰酸钾溶液鉴别苯、环已烯和环已烷
C.用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯
D.用燃烧法鉴别乙醇、苯和四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
纸层析法分离铁离子和铜离子的实验中,正确的操作是
A.在滤纸上点样时,试样点以稍大为宜
B.应沿试管壁小心地将展开剂慢慢倒入试管底部
C.将滤纸上的试样点浸入展开剂中
D.点样后的滤纸需晾干后,才能将其浸入展开剂中
查看答案和解析>>
科目:高中化学 来源: 题型:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,
反应的化学方程式如下:
2NH3(g)+CO2(g)  NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0
(1)如用右图装置制取氨气,你所选择的试剂是 。

(2)制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。

注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是: 、 。液体石蜡鼓泡瓶的作用是: 。
②从反应后的混合物中分离出产品,为了得到干燥产品,应采取的方法是_______ (填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
③尾气处理装置如右图所示。双通玻璃管的作用: ;
浓硫酸的作用: 、 。

(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品11.73 g,用足量石灰水 充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为15.00 g。则样品中氨基甲酸铵的物质的量分数为 。
[Mr(NH2COONH4)=78g/mol、Mr(NH4HCO3) =79 g/mol、Mr(CaCO3)=100 g/mol]【来.源:全,
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中A、B、C、D、E、F、G均为有机化合物。根据下图回答下列问题。

(1)D的化学名称是__________。
(2)反应③的化学方程式是________________________________。
(有机物须用结构简式表示)
(3)B的分子式是____________;A的结构式是______________;反应①的反应类型是____________。
(4)符合下列3个条件的B的同分异构体的数目有______种。
(Ⅰ)为邻位取代苯环结构;(Ⅱ)与B具有相同官能团;
(Ⅲ)不与FeCl3溶液发生显色反应。
写出其中任意一种同分异构体的结构简式____________________________________。
(5)G是重要的工业原料,用化学方程式表示G的一种重要的工业用途
_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
大气中的部分碘源于O3对海水中I-的氧化。将O3持续通入NaI溶液中进行模拟研究。
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+O3(g)===IO-(aq)+O2(g) ΔH1
②IO-(aq)+H+(aq)HOI(aq) ΔH2
③HOI(aq)+I-(aq)+H+(aq)I2(aq)+H2O(l) ΔH3
总反应的化学方程式为__________________,其反应热ΔH=_______。

(2)在溶液中存在化学平衡:I2(aq)+I-(aq)I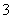 (aq),其平衡常数表达式为________。
(aq),其平衡常数表达式为________。
(3)为探究Fe2+对O3氧化I-反应的影响(反应体系如图甲),某研究小组测定两组实验中I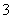 浓度和体系pH,结果见图乙和下表。
浓度和体系pH,结果见图乙和下表。
| 编号 | 反应物 | 反应前pH | 反应后pH |
| 第1组 | O3+I- | 5.2 | 11.0 |
| 第2组 | O3+I-+Fe2+ | 5.2 | 4.1 |
①第1组实验中,导致反应后pH升高的原因是______________。
②图甲中的A为________。由Fe3+生成的A的过程能显著提高I-的转化率,原因是____________________________________________________。
③第2组实验进行18 s后,I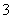 浓度下降。导致下降的直接原因有(双选)________。
浓度下降。导致下降的直接原因有(双选)________。
A.c(H+)减小 B.c(I-)减小
C.I2(g)不断生成 D.c(Fe3+)增加
(4)据图乙,计算3~18 s内第2组实验中生成I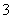 的平均反应速率(写出计算过程,结果保留两位有效数字)。
的平均反应速率(写出计算过程,结果保留两位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com