
| A、氧化铝可以用来制造耐火坩埚、耐火管和耐高温的实验仪器 |
| B、氢氧燃料电池、铅蓄电池、硅太阳能电池中都利用了原电池原理 |
| C、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| D、氨气溶于水显碱性,可以用湿润的红色石蕊试纸检验氨气的生成 |


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
| 溶解 |
| ① |
| BaCl2 |
| ② |
| NaOH |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
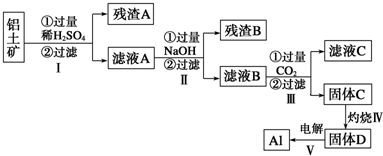
- 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al(OH)3既能够与盐酸反应又能够与NaOH溶液反应 |
| B、这种吸附剂也能吸附色素 |
| C、向Al2(SO4)3溶液中加入过量的NaOH溶液也能得到Al(OH)3 |
| D、实验室中Al(OH)3可以由可溶性铝盐溶液与足量的氨水反应制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:
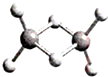 近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法错误的是( )
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法错误的是( )| A、氢铝化合物与水反应生成氢氧化铝和氢气 |
| B、Al2H6中含有离子键和极性共价键 |
| C、氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| D、氢铝化合物中可能存在组成为AlnH2n+2的物质(n为正整数) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- |
| B、水电离出的c(H+)=1×10-10的溶液中:K+、HCO3-、Na+、S2- |
| C、使pH试纸显深蓝色的溶液中:Cu2+、Fe3+、NO3-、SO42- |
| D、能与金属铝反应放出氢气的溶液:Mg2+、SO42-、NO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com