
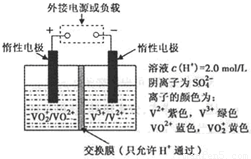
 2SO3
2SO3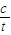 =
= =
=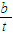 mol/��L?min��
mol/��L?min�� mol/��L?min����
mol/��L?min����

 һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д� Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| b |
| t |
| b |
| t |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����V�����仯����㷺Ӧ���ڹ�ҵ�����²��Ϻ�����Դ������V2O5�ǽӴ���������Ĵ�����
����V�����仯����㷺Ӧ���ڹ�ҵ�����²��Ϻ�����Դ������V2O5�ǽӴ���������Ĵ�����| b |
| t |
| b |
| t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 3 |
| 2 |
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| b |
| t |
| b |
| t |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ���Ĵ��ɶ������ѧУ����10���¿���ѧ�� ���ͣ������
����V�����仯����㷺Ӧ���ڹ�ҵ�����²��Ϻ�����Դ������V2O5�ǽӴ���������Ĵ�����
��1�� һ�������£�SO2 �������Ӧt min��SO2 ��SO3 ���ʵ���Ũ�ȷֱ�Ϊa mol/L��b mol��L��1����SO2 ��ʼ���ʵ���Ũ��Ϊ_________mol/L ������SO3�Ļ�ѧ��Ӧ����Ϊ_____________________��
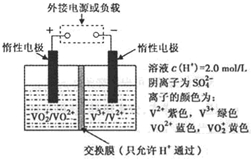
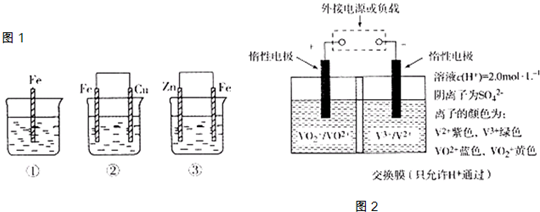
��2��ȫ��Һ�����ܵ�������ò�ͬ��̬���Ӷ�������ԭ��Ӧ��ʵ�ֻ�ѧ�ܺ͵����ת���ģ���װ��ԭ������ͼ��
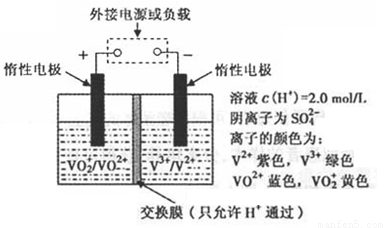
�� �������Һ���ɻƱ�������缫��ӦʽΪ_______________________________��
�� �������У��Ҳ���Һ��ɫ����__________ɫ��Ϊ_______ɫ��
�� �ŵ�����������ӵ�������________________��___________________________�����ʱ��ת�Ƶĵ�����Ϊ3.01��1023���������Һ��n(H+)�ı仯��Ϊ______________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com