

分析 反应①:富铁铝土矿(主要含有A12O3、Fe2O3、FeO和SiO2)用氢氧化钾溶液溶解,氧化铝、二氧化硅反应溶解,过滤,溶液A主要含有KAlO2、K2SiO3,滤渣A为Fe2O3、FeO,
反应②为主要含有KAlO2、K2SiO3的溶液A与稀硫酸反应生成H2SiO3白色胶状沉淀和硫酸铝和硫酸钾溶液,对溶液蒸发浓缩、冷却结晶得到明矾,
反应③滤渣A主要含有Fe2O3、FeO,用硫酸处理,得到溶液B中含有Fe2(SO4)3、FeSO4及未反应的硫酸等,加入足量X后冷却、结晶、过滤得到FeSO4•7H2O,则X为Fe,将Fe3+转化为Fe2+,过滤过量的铁,滤液为FeSO4溶液,用蒸发浓缩、冷却结晶得到FeSO4•7H2O,据此分析解答.
解答 解:(1)经过操作1得到溶液和滤渣,分离固液的操作为过滤;
故答案为:过滤;
(2)反应①②③均为复分解反应,反应④为铁还原铁离子的反应;
故答案为:④;
(3)溶液B中含有Fe2(SO4)3、FeSO4及未反应的硫酸等,加入足量X后冷却、结晶、过滤得到FeSO4•7H2O,则X为Fe,将Fe3+转化为Fe2+,反应为:Fe+2Fe3+=3Fe2+;
故答案为:Fe;Fe+2Fe3+=3Fe2+;
(4)反应①为富铁铝土矿中用氢氧化钾溶液溶解,氧化铝、二氧化硅反应溶解生成偏铝酸钠、硅酸钠,离子方程式为:SiO2+2OH-=SiO32-+H2O;Al2O3+2OH-=2AlO2-+H2O;
故答案为:SiO2+2OH-=SiO32-+H2O;Al2O3+2OH-=2AlO2-+H2O;
(5)根据分析溶液D的金属阳离子为Fe2+;检验亚铁离子的方法为:取少量溶液D于试管中,滴入硫氰化钾溶液,无现象;再滴入几滴氯水,若变红;证明含有Fe2+;
故答案为:Fe2+;检验亚铁离子的方法为:取少量溶液D于试管中,滴入硫氰化钾溶液,无现象;再滴入几滴氯水,若变红;证明含有Fe2+;
(6)用含铝元素27%的上述矿石10吨,设通过上述流程最多生产明矾质量为x,则有$\frac{27}{474}×x$=27%×10t,解得x=47.4t;
故答案为:47.4.
点评 本题综合考查物质制备实验,关键是对工艺流程原理的理解,注意分析工艺流程中试剂线、原理线、操作线,要求学生具有一定分析和解决问题的能力,题目难度中等.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 为除去酸性CuCl2溶液中含有的少量Fe3+,可在加热、搅拌的条件下加入氨水,过滤后,再向滤液中加入适量盐酸 | |
| B. | 在工业合成NH3的反应中,采取高温措施 | |
| C. | 恒温下,对平衡体系H2(g)+Br2(g)?2HBr(g)加压,可使气体颜色变深 | |
| D. | 向饱和氯化钠溶液中不断缓慢地通入HCl气体,会析出晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电负性:④>③>②>① | B. | 原子半径:④>③>②>① | ||
| C. | 第一电离能:④>③>②>① | D. | 最高正化合价:④>③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Sr为于第4周期ⅡA 族 | |
| B. | ${\;}_{38}^{90}$Sr核内中子数与质子数之差为14 | |
| C. | ${\;}_{38}^{90}$Sr与${\;}_{39}^{90}$Y互为同位素 | |
| D. | ${\;}_{38}^{90}$Sr的核内质子数为38,Sr元素的相对原子质量为90 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1标准大气压下原子数为NA的水蒸气为1mol | |
| B. | 1L1mol/L的NaOH溶液中Na+的物质的量为1mol | |
| C. | 标准状况下,22.4L氦气的质量为4g | |
| D. | 用含1molHCl的盐酸制取氯气,氯元素失去的电子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 | |
| B. | 用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度 | |
| C. | 用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 | |
| D. | 金属发生吸氧腐蚀时,被腐蚀的速率与氧气浓度无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
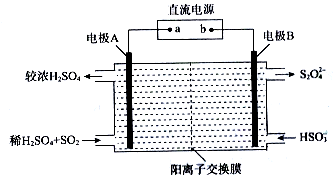
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com