
øł¾Ż±ķÖŠŠÅĻ¢£¬ÅŠ¶ĻŅŌĻĀŠšŹöÕżČ·µÄŹĒ
²æ·Ö¶ĢÖÜĘŚŌŖĖŲµÄŌ×Ó°ė¾¶¼°Ö÷ŅŖ»ÆŗĻ¼Ū
| ŌŖĖŲ“śŗÅ | L | M | Q | R | T |
| Ō×Ó°ė¾¶£Ænm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| Ö÷ŅŖ»ÆŗĻ¼Ū | £«2 | £«3 | £«2 | £«6”¢£2 | £2 |
A£®Ēā»ÆĪļµÄĪČ¶ØŠŌĪŖH2T£¼H2R”””””” B£®µ„ÖŹÓėĻ”ŃĪĖį·“Ó¦µÄ¾ēĮŅ³Ģ¶ČĪŖL£¼Q
C£®MÓėTŠĪ³ÉµÄ»ÆŗĻĪļ¾ßÓŠĮ½ŠŌ D£®L2+ÓėR2£µÄŗĖĶāµē×ÓŹżĻąµČ
 Ö„ĀéæŖ»ØæĪ³ĢŠĀĢåŃéĻµĮŠ“š°ø
Ö„ĀéæŖ»ØæĪ³ĢŠĀĢåŃéĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
æÉÄę·“Ó¦N2£«3H22NH3ŹĒ¹¤ŅµÉĻŗĻ³É°±µÄÖŲŅŖ·“Ó¦”£
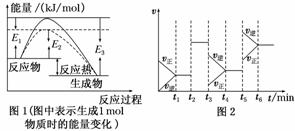
(1)øł¾ŻĶ¼1ĒėŠ“³öŗĻ³É°±µÄČČ»Æѧ·½³ĢŹ½
________________________________________________________________________
________________________________________________________________________
(ČČĮæÓĆE1”¢E2»ņE3±ķŹ¾)”£
(2)Ķ¼1ÖŠŠéĻß²æ·ÖŹĒĶعżøıä»Æѧ·“Ó¦ÖŠµÄ________Ģõ¼ž£¬øĆĢõ¼žµÄøıäÓėĶ¼2ÖŠÄÄŅ»Ź±æĢĢõ¼žµÄøıäĻąĶ¬________(ÓĆ”°t1””t6”±±ķŹ¾)”£
(3)Ķ¼2ÖŠt3Ź±æĢøıäµÄĢõ¼žŹĒ________________£¬t5Ź±æĢøıäµÄĢõ¼žŹĒ________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ŲÓŚ»ÆŗĻ¼ŪµÄĖµ·ØÕżČ·µÄŹĒ£Ø£©
| A£® | ŌŚNa2OÖŠ£¬ÄĘŌ×ÓĻŌ+1¼Ū£¬ŃõŌ×ÓĻŌ©2¼Ū | |
| B£® | ŌŚO2ÖŠ£¬ŃõŌŖĖŲĻŌ©2¼Ū | |
| C£® | ·Ē½šŹōŌŖĖŲŌŚ»ÆŗĻĪļÖŠ×ÜĻŌøŗ¼Ū | |
| D£® | Ņ»ÖÖŌŖĖŲŌŚĶ¬Ņ»ÖÖ»ÆŗĻĪļÖŠ£¬æÉÄÜÓŠ¼øÖÖ»ÆŗĻ¼Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÖĘČĖŌģ½šøÕŹÆSiCµÄ»Æѧ·½³ĢŹ½ŹĒ£ŗSiO2+3C SiC+2CO”ü£¬°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
SiC+2CO”ü£¬°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Öø³öŃõ»Æ¼Į”¢»¹Ō¼ĮŗĶŃõ»Æ²śĪļ£®
£Ø2£©±ź³öµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄ森
£Ø3£©ÓĆ30gSiO2ŗĶ24gCÄÜÖʵƶąÉŁæĖSiC£æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A”¢B”¢CČżÖÖŌŖĖŲµÄŌ×ÓŠņŹżŅĄ“ĪĪŖa”¢b”¢c£¬ĖüĆĒµÄĄė×ÓAn+”¢Bn-”¢Cm-¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬ĒŅn > m £¬ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ
A£®a > b > c B£®a > c > b
C£®a = b + m + n D£®a = c ØC n - m
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŹµŃéĢ½¾æŹĒĢåŃéÖŖŹ¶µÄ²śÉś»ņŠĪ³É¹ż³ĢµÄ»ł±¾Ķ¾¾¶£®ĻĀĆęŹĒijĶ¬Ń§Ģ½¾æŹµŃé±ØøęµÄŅ»²æ·Ö£¬ĒėĢīæÕ£ŗŹµŃéÄæµÄ£ŗĀČ”¢ä唢µāµÄŃõ»ÆŠŌĒæČõ±Č½Ļ
ŹµŃéŅ©Ę·£ŗNaClČÜŅŗ”¢KBrČÜŅŗ”¢KIČÜŅŗ”¢ĀČĖ®”¢äåĖ®”¢ĖÄĀČ»ÆĢ¼
| ŹµŃé²½Öč | ½įĀŪ |
| ¢ŁNaClČÜŅŗ+ĀČĖ®+1mL CCl4£¬Õńµ“£¬¾²ÖĆ£¬¹Ū²ģĖÄĀČ»ÆĢ¼²ćŃÕÉ« | Ńõ»ÆŠŌ“ÓĒæµ½ČõµÄĖ³Šņ£ŗ ĀČ”¢ä唢µā |
| ¢ŚKBrČÜŅŗ+ĀČĖ®+1mL CCl4£¬Õńµ“£¬¾²ÖĆ£¬¹Ū²ģĖÄĀČ»ÆĢ¼²ćŃÕÉ« | |
| ¢ŪKIČÜŅŗ+ĀČĖ®+1mL CCl4£¬Õńµ“£¬¾²ÖĆ£¬¹Ū²ģĖÄĀČ»ÆĢ¼²ćŃÕÉ« |
£Ø1£©Ķź³ÉøĆŹµŃéŠčÓƵ½µÄŅĒĘ÷ŹĒ______£»
£Ø2£©CCl4ŌŚŹµŃéÖŠĖłĘšµÄ×÷ÓĆŹĒ______£»
£Ø3£©ŌŚŹµŃé¢ŚÖŠĖÄĀČ»ÆĢ¼²ćŃÕÉ«±ä»Æ¹ż³ĢĪŖ______£»
£Ø4£©øĆĶ¬Ń§µÄŹµŃéȱĻŻŹĒ______£¬øĽųµÄ°ģ·ØŹĒ______£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
X”¢Z”¢Q”¢R”¢T”¢U·Ö±š“ś±ķŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚŌŖĖŲ”£XŗĶRŹōĶ¬×åŌŖĖŲ£»ZŗĶUĪ»ÓŚµŚVIIA×壻XŗĶZæÉŠĪ³É»ÆŗĻĪļXZ4£»Q»łĢ¬Ō×ÓµÄs¹ģµĄŗĶp¹ģµĄµÄµē×Ó×ÜŹżĻąµČ£»TµÄŅ»ÖÖµ„ÖŹŌŚæÕĘųÖŠÄܹ»×ŌČ¼”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©R»łĢ¬Ō×ӵĵē×ÓÅŲ¼Ź½ŹĒ_____________________”£
£Ø2£©ĄūÓĆ¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻTU3µÄĮ¢Ģå¹¹ŠĶŹĒ______”£
£Ø3£©XĖłŌŚÖÜĘŚŌŖĖŲ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÖŠ£¬ĖįŠŌ×īĒæµÄŹĒ______(Ģī»ÆѧŹ½)£»ZŗĶUµÄĒā»ÆĪļÖŠ·Šµć½ĻøߵďĒ_____(Ģī»ÆѧŹ½)£»Q”¢R”¢UµÄµ„ÖŹŠĪ³ÉµÄ¾§Ģ壬ČŪµćÓÉøßµ½µĶµÄÅÅĮŠĖ³ŠņŹĒ_______(Ģī»ÆѧŹ½)”£
 £Ø4£©CuSO4ČÜŅŗÄÜÓĆ×÷T4ÖŠ¶¾µÄ½ā¶¾¼Į£¬·“Ó¦æÉÉś³ÉTµÄ×īøß¼Ūŗ¬ŃõĖįŗĶĶ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_______________________”£
£Ø4£©CuSO4ČÜŅŗÄÜÓĆ×÷T4ÖŠ¶¾µÄ½ā¶¾¼Į£¬·“Ó¦æÉÉś³ÉTµÄ×īøß¼Ūŗ¬ŃõĖįŗĶĶ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷×éĪļÖŹ£¬»„ĪŖĶ¬·ÖŅģ¹¹ĢåµÄŹĒ
A£®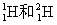 B£®O2ŗĶO3
B£®O2ŗĶO3
|
|
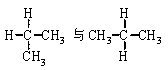 D£®
D£®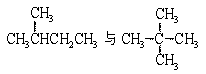
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com