
| A£®·Šµć£ŗHCl < HF < H2O |
| B£®Ąė×Ó°ė¾¶“󊔣ŗCl£>S2£>K+ |
| C£®ŅŃÖŖKsp(AgCl)>Ksp(AgBr),ŌņAgBr²»æÉÄÜ×Ŗ»Æ³ÉAgCl |
D£®½įŗĻH+µÄÄÜĮ¦£ŗ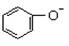 > CO32£> CH3COO£ > CO32£> CH3COO£ |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
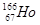 æÉÓŠŠ§µŲÖĪĮĘøĪ°©£¬øĆĶ¬Ī»ĖŲŌ×ÓŗĖÄŚµÄÖŠ×ÓŹż
æÉÓŠŠ§µŲÖĪĮĘøĪ°©£¬øĆĶ¬Ī»ĖŲŌ×ÓŗĖÄŚµÄÖŠ×ÓŹż| A£®99 | B£®67 | C£®166 | D£®233 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®12CŗĶ14C»„ĪŖĶ¬Ī»ĖŲ |
B£®Õż¶”Ķé(CH3CH2CH2CH3)ŗĶŅģ¶”Ķé(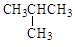 )µÄ·Ö×ÓŹ½ĻąĶ¬ )µÄ·Ö×ÓŹ½ĻąĶ¬ |
| C£®¶žŃõ»ÆĢ¼ŗĶøɱł»„ĪŖĶ¬ĖŲŅģŠĪĢå |
| D£®ŅŅ“¼(CH3CH2OH)Óė¶ž¼×ĆŃ£ØCH3-O-CH3£©»„ĪŖĶ¬·ÖŅģ¹¹Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®»Æѧ·“Ó¦¼Č×ńŹŲ”°ÖŹĮæŹŲŗć”±¶ØĀÉ£¬Ņ²×ńŹŲ”°ÄÜĮæŹŲŗć”±¶ØĀÉ |
| B£®HF”¢HCl”¢HBr”¢HIµÄµÄĪČ¶ØŠŌŅĄ“ĪŌöĒæ |
| C£®·²µ„Ō×ÓŠĪ³ÉµÄĄė×Ó£¬Ņ»¶Ø¾ßÓŠĻ”ÓŠĘųĢåŌŖĖŲŌ×ÓµÄŗĖĶāµē×ÓÅŲ¼ |
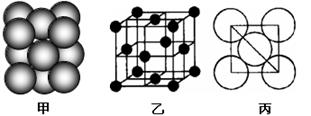
| D£®Į½ÖÖĮ£×Ó£¬Čē¹ūŗĖĶāµē×ÓÅŲ¼ĻąĶ¬£¬ŌņĖüĆĒ»„ĪŖĶ¬Ī»ĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| a | | | |||||||||||||||
| b | | | | c | d | e | f | | |||||||||
| g | h | i | j | | k | l | m | ||||||||||
| n | | | | | | | o | | | | | | | | | | |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com