
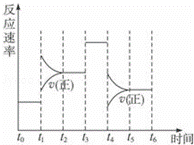
在一密闭体系中发生下列反应A(g)+3B(g)⇌2C(g)△H<0,如图是某一时间段中反应速率与反应进程的曲线关系,完成下列问题:
(1)t1、t3、t4时刻体系中所改变的条件可能是: 、 、 ;
(2)C体积分数最高的时间段是 .(填“tx﹣ty”)
考点:
化学反应速率变化曲线及其应用.
专题:
化学平衡专题.
分析:
(1)根据温度、催化剂以及压强对反应速率的影响分析,注意各时间段正逆反应速率的变化;
(2)t1~t2,t4~t5,反应向逆反应方向移动,随着反应的进行,生成的C逐渐减小,C的体积分数逐渐减小.
解答:
解:(1)t1时,正逆反应速率都增大,且逆反应速率大于正反应速率,反应向逆反应方向移动,则应为升高温度的变化,
t3时,正逆反应速率都增大,正逆反应速率相等,平衡不移动,应为加入催化剂的变化,
t4时,正逆反应速率都减小,且逆反应速率大于正反应速率,平衡向逆反应方向移动,由方程式计量数关系可知,应为减小压强的变化,
故答案为:升温;使用正催化剂;减压;
(2)t1~t2,t4~t5,反应向逆反应方向移动,随着反应的进行,生成的C逐渐减小,C的体积分数逐渐减小,故C体积分数最高的时间段是t0~t1,故答案为:t0~t1.
点评:
本题考查化学反应速率的变化曲线,题目难度中等,注意化学方程式的特点,判断温度、压强对反应平衡移动的影响,结合外界条件对反应速率的影响分析.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
中科院化学所研制的晶体材料﹣﹣纳米四氧化三铁,在核磁共振造影及医药上有广泛用途其生产过程的部分流程如下:FeCl3•6H2O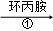 FeOOH
FeOOH 纳米四氧化三铁,下列有关叙述不合理的是()
纳米四氧化三铁,下列有关叙述不合理的是()
A. 纳米四氧化三铁可分散在水中,它与FeCl3溶液的分散质直径相当
B. 纳米四氧化三铁具有磁性,可作为药物载体用于治疗疾病
C. 在反应①中环丙胺的作用可能是促进氯化铁水解
D. 反应②的化学方程式是6FeOOH+CO=2Fe3O4+3H2O+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解.
(2)把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是 .
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关热化学方程式的叙述正确的是( )
|
| A. | 2H2(g)+O2(g)═2H2O(g)△H=﹣483.6 kJ/mol,则氢气的燃烧热为241.8 kJ |
|
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
|
| C. | 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=﹣57.4 kJ/mol |
|
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2.则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个固定体积为2升的密闭容器中,充入2mol A和1mol B,发生如下反应:2A(g)+B(g)⇌3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L.
(1)2分钟内用B表示的平均反应速度为 ;
(2)若容器温度升高,平衡时混合气体的平均相对摩尔质量减小,则正反应为: (填“吸热”或“放热”)反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
据科学家预测,月球的土壤中吸附着数百万吨的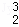 He,每百吨
He,每百吨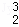 He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上氦元素主要以
He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上氦元素主要以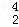 He的形式存在.下列说法正确的是()
He的形式存在.下列说法正确的是()
A. 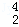 He原子核内含有4个质子
He原子核内含有4个质子
B. 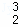 He原子核内含有3个中子
He原子核内含有3个中子
C. 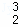 He和
He和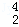 He互为同位素
He互为同位素
D. 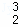 He和
He和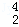 He互为同素异形体
He互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X和Y组成原电池时,Y为电池的负极.X、Y、Z三种金属的活动性顺序为()
A. X>Y>Z B. X>Z>Y C. Y>X>Z D. Y>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
今有0.1mol/L Na2SO4溶液300mL,0.1mol/L MgSO4溶液200mL和0.1mol/L Al2(SO4)3溶液100mL,这三种溶液中硫酸根离子的物质的量之比是()
A. 1:1:1 B. 3:2:2 C. 3:2:3 D. 1:1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
传统合成氨工业需要采用高温、高压和催化剂.近来美国化学家使用新型铁系催化剂,在常温下合成了氨气.下列说法正确的是()
A. 新型合成氨方法是吸热反应
B. 新型合成氨方法可简化生产设备
C. 新型催化剂提高了N2和H2的转化率
D. 两种方法中该反应的化学平衡常数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com