
某化学兴趣小组的同学为进行物质性质的探究,用维持烧瓶内压强与分液漏斗内压强相等,使液体能顺利滴下
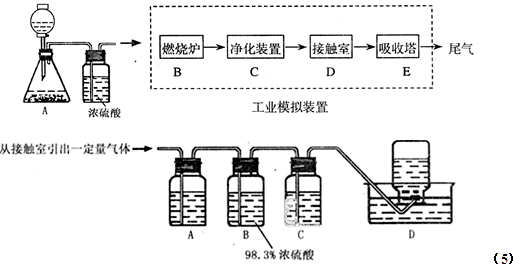
下图所示装置进行实验。请回答下列问题:(加热及固定装置已略去)

(1)装置A中反应的化学方程式为
(2)装置C 中的试剂是 ( 填序号).
A.氢氧化钠溶液 B. 酸性高锰酸钾溶液 C.亚硫酸氢钠溶液
发生反应的离子方程式为 ,其说明了SO2具有 ,该实验操作的名称是 。
(3)在上述实验中,能说明碳的非金属性比硅强的实验现象是
(4)B中的溶液无明显现象,当滴加氯水时有白色沉淀,写出SO2表现还原性并生成白色沉淀的总离子方程式为
(1)Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O(2)B 2MnO4-+5SO2+2H2O═2Mn2++5SO42-+4H+,还原性,洗气。(3)E中的品红溶液不褪色,F中有白色沉淀。 (4)Ba2++Cl2+2H2O+SO2= BaSO4↓+4H+
+2 Cl-
CuSO4+SO2↑+2H2O(2)B 2MnO4-+5SO2+2H2O═2Mn2++5SO42-+4H+,还原性,洗气。(3)E中的品红溶液不褪色,F中有白色沉淀。 (4)Ba2++Cl2+2H2O+SO2= BaSO4↓+4H+
+2 Cl-
【解析】
试题分析:(1)反应装置A中为浓硫酸与铜在加热条件下反应,故反应方程式为Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
(2)A选项,氢氧化钠与二氧化硫无现象,错误。B选项,正确,二氧化硫具有还原性,能使酸性高锰酸钾溶液褪色,可验证二氧化硫的还原性。C选项,不发生反应。无现象。错误。故选择B选项。离子反应方程式为2MnO4-+5SO2+2H2O═2Mn2++5SO42-+4H+。溶液褪色,证明二氧化硫具有还原性。操作名称为洗气。(3)在D反应器中,二氧化硫与碳酸氢钠溶液发生反应,产生二氧化碳,到达E反应器中,二氧化碳不能使品红褪色,但二氧化碳可以和硅酸钠溶液反应,产生硅酸沉淀,可证明碳酸的酸性强于硅酸,故碳的非金属性强于硅的非金属性。故实验现象为 E中的品红不褪色,F中有白色沉淀生成。(4)B中通入氯气,可将亚硫酸根氧化为硫酸根,产生白色沉淀。故其反应方程式为Ba2++Cl2+2H2O+SO2= BaSO4↓+4H+
+2 Cl-。
CuSO4+SO2↑+2H2O
(2)A选项,氢氧化钠与二氧化硫无现象,错误。B选项,正确,二氧化硫具有还原性,能使酸性高锰酸钾溶液褪色,可验证二氧化硫的还原性。C选项,不发生反应。无现象。错误。故选择B选项。离子反应方程式为2MnO4-+5SO2+2H2O═2Mn2++5SO42-+4H+。溶液褪色,证明二氧化硫具有还原性。操作名称为洗气。(3)在D反应器中,二氧化硫与碳酸氢钠溶液发生反应,产生二氧化碳,到达E反应器中,二氧化碳不能使品红褪色,但二氧化碳可以和硅酸钠溶液反应,产生硅酸沉淀,可证明碳酸的酸性强于硅酸,故碳的非金属性强于硅的非金属性。故实验现象为 E中的品红不褪色,F中有白色沉淀生成。(4)B中通入氯气,可将亚硫酸根氧化为硫酸根,产生白色沉淀。故其反应方程式为Ba2++Cl2+2H2O+SO2= BaSO4↓+4H+
+2 Cl-。
考点:离子反应方程式,二氧化硫的性质实验。


科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验 | 实验操作 | 现象 | 结论 |
| I | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物具有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 实验 序号 |
实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气体产生 | 氯气与水反应的产物具有酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 实验步骤 |
| ① | 将镁条用砂纸打磨后,放入沸水中,再向溶液中滴加酚酞溶液 |
| ② | 向新制得到的Na2S溶液中滴加新制的氯水 |
| ③ | 将一小块金属钠放入滴有酚酞溶液的冷水中 |
| ④ | 将镁条投入稀盐酸中 |
| ⑤ | 将铝条投入稀盐酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| 压强/Mpa 转化率 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com