
【题目】工业生产过程中处处体现化学变化的无穷魅力,请用化学方程式说明下列变化.
(1)在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:向废液中投入过量铁屑,充分反应后分离出固体和滤液;向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气.FeCl3蚀刻铜箔反应的离子方程式为 , 鼓入空气时的化学方程式为 .
(2)铝土矿(主要成分是Al2O3)在提炼时首先用NaOH溶液溶解,其离子方程式为 .
(3)工业上制得 NO的化学方程式 . 氮氧化物(NO和NO2)污染环境,若用Na2CO3溶液吸收NO和NO2(两种气体体积之比1:1),可生成CO2和一种盐.则反应的离子方程式为 .
【答案】
(1)2Fe3++Cu=2Fe2++Cu2+;4Fe(OH)2+O2+2H2O=4Fe(OH)3
(2)Al2O3+2OH﹣=2AlO2﹣+H2O
(3)4NH3+5O2 ![]() 4NO+6H2O;NO+NO2+CO32﹣=CO2+2NO2﹣
4NO+6H2O;NO+NO2+CO32﹣=CO2+2NO2﹣
【解析】解:(1)FeCl3蚀刻铜箔反应生成氯化亚铁、氯化铜,离子反应为2Fe3++Cu=2Fe2++Cu2+;鼓入空气时氢氧化亚铁被氧化生成氢氧化铁,发生的反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3 ,
所以答案是:2Fe3++Cu=2Fe2++Cu2+;4Fe(OH)2+O2+2H2O=4Fe(OH)3;(2)氧化铝与NaOH反应生成偏铝酸钠和水,离子反应为Al2O3+2OH﹣=2AlO2﹣+H2O,所以答案是:Al2O3+2OH﹣=2AlO2﹣+H2O;(3)氨气催化氧化生成NO,反应为4NH3+5O2 ![]() 4NO+6H2O;用Na2CO3溶液吸收NO和NO2(两种气体体积之比1:1),可生成CO2和一种盐,由氧化还原反应原理可知生成盐为NaNO2 , N元素的化合价为+3价,在+2、+4之间,离子反应为NO+NO2+CO32﹣=CO2+2NO2﹣ ,
4NO+6H2O;用Na2CO3溶液吸收NO和NO2(两种气体体积之比1:1),可生成CO2和一种盐,由氧化还原反应原理可知生成盐为NaNO2 , N元素的化合价为+3价,在+2、+4之间,离子反应为NO+NO2+CO32﹣=CO2+2NO2﹣ ,
所以答案是:4NH3+5O2 ![]() 4NO+6H2O;NO+NO2+CO32﹣=CO2+2NO2﹣ .
4NO+6H2O;NO+NO2+CO32﹣=CO2+2NO2﹣ .


科目:高中化学 来源: 题型:
【题目】下列有关高分子材料的说法中,不正确的是( )
A.聚氯乙烯在建筑材料、人造革、管材、食品包装膜等方面均有广泛应用
B.橡胶硫化可提高橡胶制品的强度,汽车轮胎使用的便是硫化橡胶
C.高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工、酿造业等
D.人造器官使用的是生物医用仿生高分子材料,具有较好的生物相容性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁:另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的物质的量浓度为( )
A.(4b﹣2a)/V molL﹣1
B.(b﹣2a)/V molL﹣1
C.(2b﹣2a)/V molL﹣1
D.(b﹣a)/V molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过反应“SiO2+2C![]() Si+2CO↑”制取单质硅,下列说法正确的是
Si+2CO↑”制取单质硅,下列说法正确的是
A. 自然界中硅元素均以SiO2形式存在
B. 高纯度晶体Si可用于制造光导纤维
C. 该反应条件下C的还原性比Si强
D. 标准状况下生成4.48 L CO时转移电子数为0.4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO,Fe2O3的混合物中,加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况下)的气体,所得溶液中加入KSCN溶液无血红色出现,则原混合物中铁元素的质量为( )
A.5.6g
B.2.8g
C.11.2g
D.1.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定放置已久的小苏打样品中纯碱的质量分数.
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算.实验中加热至恒重的目的是 .
(2)方案二:按如图装置进行实验.并回答以下问题: 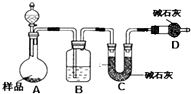
①分液漏斗中应该装(填“盐酸”或“稀硫酸盐”),D装置的作用是 .
②实验中除称量样品质量外,还需称装置反应前后质量的变化(用装置的字母代号);
③根据此实验得到的数据,测定结果有较大误差,因为实验装置还存在一个明显缺陷,该缺陷是 .
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤洗涤,干燥沉淀,称量固体质量,计算:
①实验中判断沉淀已完全的方法是 .
②若加入试剂改为氢氧化钡,已知称得样品9.5g,干燥的沉淀质量为19.7g,则样品中碳酸钠的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4mo1A和2molB进行如下反应:
3A(g)+2B(g)![]() 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后的压强之比为5:4 (相同的温度下测量), 则下列说法正确的是
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后的压强之比为5:4 (相同的温度下测量), 则下列说法正确的是
A. 该反应的化学平衡常数表达式是![]()
B. 此时,B 的平衡转化率是35%
C. 增大该体系的压强,平衡向右移动化学平衡常数增大
D. 增加C的量,B的平衡转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,在2 L的密闭容器中,气体X、Y和Z三种物质的物质的量随时间变化的曲线如图所示,下列描述正确的是
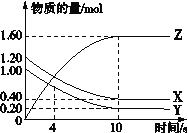
A.容器中化学反应为X(g)+Y(g)![]() Z(g)
Z(g)
B.0~10 s,X表示的平均化学反应速率为0.04 mol/(L·s)
C.使用催化剂只能加快0~10 s间的反应速率
D.0~4 s的平均反应速率小于0~10 s的平均反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com