
 ����ú��ˮ���������Ƶã�Ӧ�õ��·������磺��
����ú��ˮ���������Ƶã�Ӧ�õ��·������磺�� ��
�� ��443��473K���¶����������������ɺϳ�̼ԭ����Ϊ5��8��������
��443��473K���¶����������������ɺϳ�̼ԭ����Ϊ5��8�������� �Ļ�ѧ����ʽ
�Ļ�ѧ����ʽ ������ȫ��Ӧʱ����ѹ����ԭ����2/5�����¶Ȳ��䣩����ʱ ����С���û�С����������ɣ�������
������ȫ��Ӧʱ����ѹ����ԭ����2/5�����¶Ȳ��䣩����ʱ ����С���û�С����������ɣ�������  ������ȵ�ȡֵ��Χ��
������ȵ�ȡֵ��Χ��  ����n��ʾ
����n��ʾ ��
�� �����ʵ���֮�ȣ�a��ʾ
�����ʵ���֮�ȣ�a��ʾ ��ת���ʣ�x��ʾ�ﵽ��Ӧ��ʱ�������
��ת���ʣ�x��ʾ�ﵽ��Ӧ��ʱ������� �������������
������������� ��a��x�Ĺ�ϵʽΪ ��
��a��x�Ĺ�ϵʽΪ ��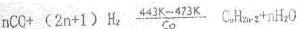 ��û��;��һ�������£�ѹǿ�ȵ������ʵ���֮�ȣ�= ��n=3���������͵�nֵ��5��11֮�䣬���˷�Ӧ��nֵΪ3���ʴ�ʱ���������ɡ���5/11��8/17(2) x=
��û��;��һ�������£�ѹǿ�ȵ������ʵ���֮�ȣ�= ��n=3���������͵�nֵ��5��11֮�䣬���˷�Ӧ��nֵΪ3���ʴ�ʱ���������ɡ���5/11��8/17(2) x=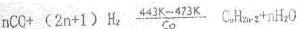 ����һ�������£�ѹǿ�ȵ������ʵ���֮�ȣ�= ��n=3���������͵�nֵ��5��11֮�䣬���˷�Ӧ��nֵΪ3���ʴ�ʱ���������ɡ���Ҫ�������ͣ���n=5ʱ����CO��H2�������Ϊ5��11����n=8ʱ����CO��H2�������Ϊ8��17����2����CO�����ʵ���ΪA��H2�����ʵ���ΪB��
����һ�������£�ѹǿ�ȵ������ʵ���֮�ȣ�= ��n=3���������͵�nֵ��5��11֮�䣬���˷�Ӧ��nֵΪ3���ʴ�ʱ���������ɡ���Ҫ�������ͣ���n=5ʱ����CO��H2�������Ϊ5��11����n=8ʱ����CO��H2�������Ϊ8��17����2����CO�����ʵ���ΪA��H2�����ʵ���ΪB��

 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO(g) + H2(g)��Ӧ��һ�������´ﵽƽ�⣬������ˮ����Ũ�ȣ�ƽ���� ��Ӧ�����ƶ�������������桱������ͬ����CO��Ũ�Ƚ� �������������С�����䡱��ͬ��
CO(g) + H2(g)��Ӧ��һ�������´ﵽƽ�⣬������ˮ����Ũ�ȣ�ƽ���� ��Ӧ�����ƶ�������������桱������ͬ����CO��Ũ�Ƚ� �������������С�����䡱��ͬ�� N2O4��g�� ������Ѹ��������ʱ��ƽ���� ��Ӧ�����ƶ����������ɫ�ȱ�_____����dz����������䡱��ͬ�������______�����պ������ȣ�_____����ǰ������
N2O4��g�� ������Ѹ��������ʱ��ƽ���� ��Ӧ�����ƶ����������ɫ�ȱ�_____����dz����������䡱��ͬ�������______�����պ������ȣ�_____����ǰ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO��g��+ H2O��g�� ��H =" Q" kJ��mol��1
CO��g��+ H2O��g�� ��H =" Q" kJ��mol��1| t�� | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
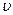 ����H2����
����H2����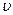 ����CO�� ��d�� CO2��������������
����CO�� ��d�� CO2�������������� CO2��g��+H2��g���ڹ̶��ݻ����ܱ������н��У������ڸ����ʵ�Ũ�ȱ仯���±���
CO2��g��+H2��g���ڹ̶��ݻ����ܱ������н��У������ڸ����ʵ�Ũ�ȱ仯���±���| ʱ�䣨min �� | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 2SO3(g)
2SO3(g)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3����H��0����ʱ�����ѱ��־�ֹ��SO2��Ӧ����Ϊv0������A��Ѹ�ٳ���2 mol SO2��1 mol O2���������ٴα��־�ֹʱ��SO2��Ӧ����Ϊv���ڴ˹����У�����˵����ȷ����
2SO3����H��0����ʱ�����ѱ��־�ֹ��SO2��Ӧ����Ϊv0������A��Ѹ�ٳ���2 mol SO2��1 mol O2���������ٴα��־�ֹʱ��SO2��Ӧ����Ϊv���ڴ˹����У�����˵����ȷ����
| A�����������ƣ������Ƶ�ԭ��ֹλ�ã�v>v0 |
| B�����������ƣ������Ƶ�ԭ��ֹλ�ã�v=v0 |
| C�����������ƣ������ƣ�����ԭ��ֹλ�ã�v>v0 |
| D�����������ƣ������ƣ�����ԭ��ֹλ�ã�v=v0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ж���

 XeF4(g)+F2(g),�䷴Ӧ�Ȧ�H0(�������������������������__________________________��
XeF4(g)+F2(g),�䷴Ӧ�Ȧ�H0(�������������������������__________________________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SCl2(�ʺ�ɫҺ��)����H=+61.16kJ��
2SCl2(�ʺ�ɫҺ��)����H=+61.16kJ��| A����λʱ��������n mol S2Cl2��ͬʱҲ����n molCl2 |
| B���ﵽƽ��ʱ���������¶ȣ�ѹǿ���䣬��Ӧ�����Һ��ɫ��dz |
| C���ﵽƽ��ʱ����λʱ��������n mol S2Cl2��ͬʱҲ����n molCl2 |
| D������������ƽ��������Ӧ�����ƶ���������ת����һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 FeO(s) �� CO(g)�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
FeO(s) �� CO(g)�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���| T(K) | 938 | 1173 |
| K | 1.47 | 2.15 |
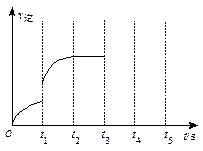
 ����t3~ t5ʱ��ε�v���仯���ߡ�
����t3~ t5ʱ��ε�v���仯���ߡ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2AB��g���ﵽƽ��״̬�ı�־��( )
2AB��g���ﵽƽ��״̬�ı�־��( )| A����λʱ��������n molA2��ͬʱ����n molAB |
| B�������ڻ�������ƽ����Է�����������ʱ��仯 |
| C����λʱ��������2n molAB��ͬʱ����n molB2 |
| D����λʱ����һ��A��A�����ѣ�ͬʱ���ɶ���A��B�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com