
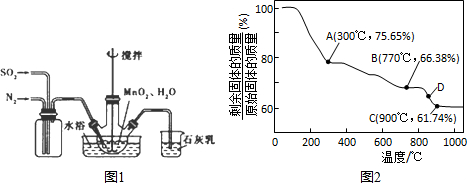
���� ��1����ѧƽ��ԭ��������֪�����ַ�Ӧ������һ�ֻ������һ������ת���ʣ�
��2����ʯ���������������β��������������������ﷴӦ�õ���Ӧ���κ�ˮ��
��ΪʹSO2������ת����ȫ��һ��Ҫ��֤���Ʒ�Ӧ���¶ȣ���ͨ��SO2��N2����һ�������ı��ҺͶ�ϵ������£�Ҫ����ͨ����һ��Ҫ����
��3������ͼ��仯��������Ϲ���ʧ�ؽ����жϸ����ʣ����壬��Ҫ�ǽ���BC��ʣ�����ɷ��ж�D��Ĺ���ɷ֣�
A��ʣ���������Ϊ115 g��75.65%=87 g
���ٵ�����Ϊ115 g-87 g=28 g
��֪MnCO3ʧȥ�����ΪCO��ʣ�����ijɷ�ΪMnO2
B��ʣ���������Ϊ115 g��66.38%=76.337 g
��m��Mn��=55 g����m��O ��2=76.337 g-55 g=21.337 g
��n��Mn����n��O��=$\frac{55}{55}$��$\frac{21.337}{16}$=3��4
��ʣ�����ijɷ�ΪMn3O4
��D�����B��C֮�䣬��D���Ӧ����ijɷ�ΪMn3O4��MnO�Ļ���
��� �⣺��1����ҵ���Ʊ�����ʽΪ��MnSO4+2NH4HCO3=MnCO3��+��NH4��2SO4+CO2��+H2O����Ӧ��ͨ��������Թ�����NH4HCO3���ҿ�����Һ��pHΪ6.8��7.4�������Թ�����NH4HCO3��Ŀ���ǣ������Թ�����NH4HCO3�����MnSO4��ת���ʣ�ʹMnCO3������ȫ��
�ʴ�Ϊ�������Թ�����NH4HCO3�����MnSO4��ת���ʣ�ʹMnCO3������ȫ��
��2���ٶ���������������Ʒ�Ӧ����������ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2ʮSO2=CaSO3+H2O��
�ʴ�Ϊ��Ca��OH��2ʮSO2=CaSO3+H2O��
�ڷ�Ӧ�����У�ΪʹSO2������ת����ȫ����ͨ��SO2��N2����һ�������ı��ҺͶ�ϵ������£��ɲ�ȡ�ĺ�����ʩ�У������ʵ����¶ȡ�����ͨ�˻�����壬
�ʴ�Ϊ�������ʵ����¶ȡ�����ͨ�˻�����壻
��3����MnCO3�����ʵ���Ϊ1 mol��������Ϊ115 g
��A��ʣ���������Ϊ115 g��75.65%=87 g
���ٵ�����Ϊ115 g-87 g=28 g
��֪MnCO3ʧȥ�����ΪCO
��ʣ�����ijɷ�ΪMnO2 ��n��Mn����n��O��=1��2��
�ʴ�Ϊ��1��2��
��C��ʣ���������Ϊ115 g��61.74%=71 g
����Ԫ���غ�֪m��Mn��=55 g����m��O ��1=71 g-55 g=16 g
��n��Mn����n��O��=$\frac{55}{55}$��$\frac{16}{16}$=1��1
��ʣ�����ijɷ�ΪMnO
ͬ����B��ʣ���������Ϊ115 g��66.38%=76.337 g
��m��Mn��=55 g����m��O ��2=76.337 g-55 g=21.337 g
��n��Mn����n��O��=$\frac{55}{55}$��$\frac{21.337}{16}$=3��4
��ʣ�����ijɷ�ΪMn3O4
��D�����B��C֮�䣬��D���Ӧ����ijɷ�ΪMn3O4��MnO�Ļ���
�ʴ�Ϊ��Mn3O4��MnO��
���� ������Ҫ�������Ʊ��ߴ�̼����ʵ�鷽������ѧʽ�ļ���ȷ���������������̣���ȷʶͼ���������ӷ�Ӧ�ı����ǽ��Ĺؼ�������ʵ���ۺ���ǿ���Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
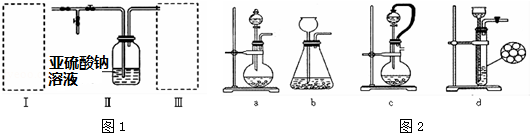
 ������������Ҫ���л��ϳ��м��壬�㷺Ӧ���ڻ�ѧ��ҵ��ijѧ����ʵ����������ͼ��ʵ��װ���Ʊ������������о��䷴Ӧ������
������������Ҫ���л��ϳ��м��壬�㷺Ӧ���ڻ�ѧ��ҵ��ijѧ����ʵ����������ͼ��ʵ��װ���Ʊ������������о��䷴Ӧ������| ���� | �е�/��C | �ܶ�/g?cm-3 |
| �Ҵ� | 78.0 | 0.79 |
| ���� | 117.9 | 1.05 |
| �������� | 77.5 | 0.90 |
| ���촼 | 131 | 0.8123 |
| ���������� | 142 | 0.8670 |
| ʵ���� | �Թܢ��е��Լ� | ����л���ĺ��/cm |
| A | 2mL�Ҵ���2mL���ᡢ1mL 18mol/LŨ���� | 5.0 |
| B | 3mL�Ҵ���2mL���� | 0.1 |
| C | 3mL�Ҵ���2mL���ᡢ6mL 3mol/L���� | 1.2 |
| D | 3mL�Ҵ���2mL���ᡢ���� | 1.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��--�٢� | B�� | ��--�٢� | C�� | ������--�ۢܢ� | D�� | �����--�ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al3+ | B�� | Ba2+ | C�� | Cl- | D�� | Mg2+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com