
把放在空气中一段时间的5.0g铝片投入盛有500mL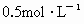 硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图坐标曲线来表示,回答下列问题:
硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图坐标曲线来表示,回答下列问题:
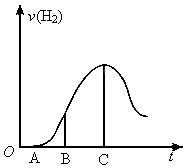
(1)曲线OA段不产生氢气的原因是_____________,有关的离子方程式是_______________.
(2)曲线AB段产生氢气的速率较慢的原因是_______________________.
(3)曲线BC段产生氢气的速率增加较快的主要原因是______________.
(4)曲线到C以后,产生氢气的速率逐渐下降的主要原因是_____________
_____________________.
 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
把放在空气中一段时间的5.0g铝片投入盛有500mL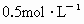 硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图坐标曲线来表示,回答下列问题:
硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图坐标曲线来表示,回答下列问题:
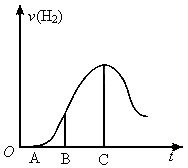
(1)曲线OA段不产生氢气的原因是_____________,有关的离子方程式是_______________.
(2)曲线AB段产生氢气的速率较慢的原因是_______________________.
(3)曲线BC段产生氢气的速率增加较快的主要原因是______________.
(4)曲线到C以后,产生氢气的速率逐渐下降的主要原因是_____________
_____________________.
查看答案和解析>>
科目:高中化学 来源:“伴你学”新课程 化学2必修(鲁科版) 题型:022
把放在空气中一段时间的5.0 g铝片投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用下图的坐标曲线来表示,回答下列问题:
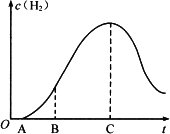
(1)曲线OA段不产生氢气的原因是________,有关的离子方程式是________.
(2)曲线AB段产生氢气的速率较慢的原因是________.
(3)曲线BC段产生氢气的速率增加较快的主要原因是________.
(4)曲线由C以后,产生氢气的速率逐渐下降的主要原因是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)以甲基橙为指示剂时,VA与VB的关系是______________________________。
(2)以酚酞为指示剂时,VA与VB的关系是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com