
| 175℃ |
| △ |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、31克白磷中,共价键数目为3NA |
| B、0.1mol 锌与100mL 1mol/L的稀盐酸充分反应,产生氢气的分子数为0.1NA |
| C、2mol SO2和1mol O2混合在(V2O5存在的条件下)密闭容器中加热反应后,容器内物质的分子数大于2NA |
| D、138gK2CO3晶体中的离子总数大于3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 2.3 | 4.0 | 7.6 |
| 完全沉淀pH | 4.1 | 5.2 | 9.6 |
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |

查看答案和解析>>
科目:高中化学 来源: 题型:
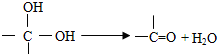
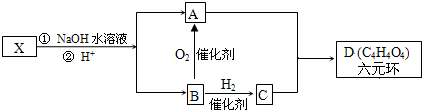
| 浓硫酸 |
| ℃170 |
| 高温、高压 |
| 催化剂 |
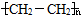 .
.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

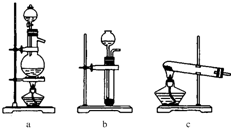

查看答案和解析>>
科目:高中化学 来源: 题型:
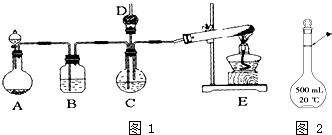 纳米碳酸钙广泛应用于橡胶、塑料、造纸、化学建材、油墨、涂料、密封胶与胶粘剂等行业.在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙.某校学生实验小组设计如图1所示装置,制取该产品.D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去.
纳米碳酸钙广泛应用于橡胶、塑料、造纸、化学建材、油墨、涂料、密封胶与胶粘剂等行业.在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙.某校学生实验小组设计如图1所示装置,制取该产品.D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“水滴石穿”可能的原因是溶解了CO2的雨水与CaCO3作用生成了可溶性Ca(HCO3)2的缘故 |
| B、25℃时,难溶物XY和AB3的Ksp分别为1.0×10-10和2.7×10-15,则该温度下,两者的饱和溶液中c(X+)一定大于c(A3+) |
| C、25℃时,pH=ll的KaA溶液和pH=11的KOH溶液,水电离的c(OH-)前者是后者的108倍 |
| D、不用其它试剂能把NaCl、AlCl3、Ba(OH)2三种溶液鉴别出来 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com