


 该反应的平衡常数表达式为 。
该反应的平衡常数表达式为 。

科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.330 kJ | B.276.67 kJ |
| C.130 kJ | D.76.67 kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
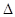 H=-67.7 kJ·mol-1
H=-67.7 kJ·mol-1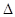 H=-57.3 kJ·mol-1
H=-57.3 kJ·mol-1A.氢氟酸的电离方程式及热效应可表示为:HF(aq) F-(aq)+H+(aq) F-(aq)+H+(aq) 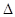 H=+10.4 kJ·mol-1 H=+10.4 kJ·mol-1 |
| B.当V=20时,溶液中:c(OH-)=c(HF)+c(H+) |
| C.当V=20时,溶液中:c(F-)<c(Na+)=0.1 mol·L-1 |
| D.当V>0时,溶液中一定存在:c(Na+)>c(F-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2HI(g) ΔH=-9.48 kJ/mol
2HI(g) ΔH=-9.48 kJ/mol  2HI(g) ΔH=+26.48 kJ/mol
2HI(g) ΔH=+26.48 kJ/mol| A.1 mol I2(g)中通入1 mol H2(g),反应放热9.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.分解1 mol HI (g)生成H2(g)和固态碘的反应吸热13.24kJ |
| D.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
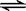 SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )| A.196.64kJ | B.98.32kJ | C.>196.64kJ | D.<196.64kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com