
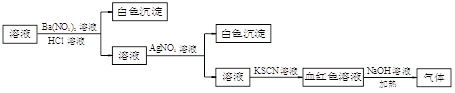
| A.原溶液中可能含有SO42— 离子 | B.原溶液中可能含有NH4+ 离子 |
| C.原溶液中一定含有Cl— 离子 | D.原溶液中一定含有Fe3+ 离子 |
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源:不详 题型:填空题
 乙
乙 丙
丙 甲
甲 丙”转化的离子方程式 。
丙”转化的离子方程式 。 乙”转化的离子方程式: 。
乙”转化的离子方程式: 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
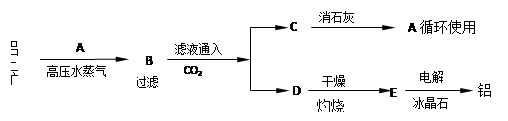
| | Al2O3 | Fe2O3 | Na2O |
| 铝土矿 | 55% | 16% | 0% |
| 赤泥 | 15% | 48% | 8% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
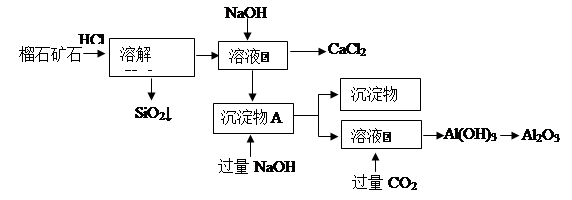
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 12.0 |
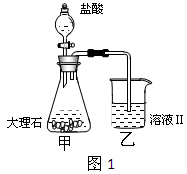
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
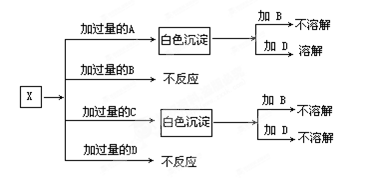
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X或Y均能使湿润的淀粉碘化钾试纸变蓝 |
| B.1molY或Z与足量水完全反应时,均转移1mol电子 |
| C.Z为离子化合物,但含有共价键,阴、阳离子个数比为1:2 |
| D.X和Y均能用向上排空气法和排水法收集 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
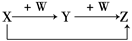 则X、W可能是( )
则X、W可能是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
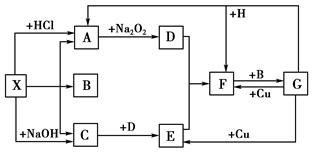
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com