
£Ø11·Ö£©£®
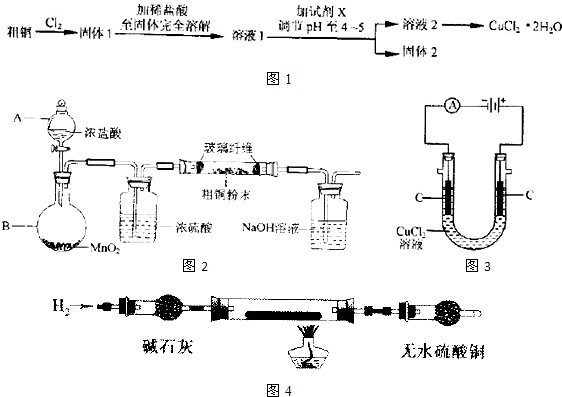
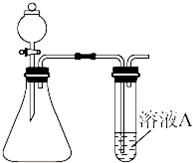
ijĶ¬Ń§²ÉÓĆČēĶ¼×°ÖĆ½ųŠŠŹµŃ飬֤Ć÷ĮĖĶÓėĻ”ĻõĖį·“Ӧɜ³ÉĮĖNO”£ŹµŃ鏱£¬ĻČĻņ×¢ÉäĘ÷ÄŚ¼ÓČėŅ»¶ØĮæµÄĻ”ĻõĖį£¬Åž»×¢ÉäĘ÷ÄŚµÄæÕĘų£¬ŃøĖŁ½«“ųÓŠĶĖæµÄĻšĘ¤Ć±øĒÉĻ£¬Ņ»¶ĪŹ±¼äŗó£¬×¢ÉäĘ÷ÄŚÓŠĪŽÉ«ĘųĢå²śÉś”£
£Ø1£©ĒėŠ“³öĶÓėĻ”ĻõĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
ӣ
£Ø2£©ČōÖ¤Ć÷ĪŽÉ«ĘųĢåŹĒNOµÄŹµŃé²Ł×÷ŗĶĻÖĻóŹĒ ”£
Ņ»Ńõ»ÆµŖŹĒ“óĘųĪŪČ¾ĪļÖ®Ņ»”£ÄæĒ°,ÓŠŅ»ÖÖÖĪĄķ·½·ØŹĒŌŚ400 ”ę×óÓŅ”¢ÓŠ“߻ƼĮ“ęŌŚµÄĒéæöĻĀ£¬ÓĆ°±°ŃŅ»Ńõ»ÆµŖ»¹ŌĪŖµŖĘųŗĶĖ®”£øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ

ĆæÓŠ10mol N2Éś³É£¬±»»¹ŌµÄŃõ»Æ¼ĮĪŖ_______mol”£
£Ø3£©Čō½«ÉĻŹöĻ”ĻõĖį»»³ÉÅØĻõĖį£¬ĘäÉś³ÉµÄĘųĢåĪŖ £¬½«“ĖĘųĢåĶØČėĖ®ÖŠ£¬·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ ”£
£Ø11·Ö£©£®
£Ø1£©3Cu + 8HNO3 = 3Cu(NO3)2 +2NO”ü+4H2O£Ø3·Ö£©£»
£Ø2£©Č”ĻĀĻšĘ¤Ć±£¬ĪŽÉ«ĘųĢå±äĪŖŗģ×ŲÉ«£Ø»ņ×¢ÉäĘ÷³öæŚ“¦ÓŠŗģ×ŲÉ«ĘųĢ壩£Ø2·Ö£©12£Ø2·Ö£©
£Ø3£©NO2 £Ø1·Ö£©”£ 3 NO2+H2O==2HNO3+NO £Ø3·Ö£©
”¾½āĪö”æ¢Å¼ū“š°ø£»¢ĘĄūÓĆNOÓėO2·“Ӧɜ³Éŗģ×ŲÉ«µÄNO2£¬¾ßĢå¼ū“š°ø£¬øĆ·“Ó¦µÄŃõ»Æ¼ĮĪŖNO£¬ÓÉ·“Ó¦Ź½ÖŖĆæÓŠ10mol N2Éś³É£¬±»»¹ŌµÄŃõ»Æ¼ĮĪŖ12mol£»¢ĒĀŌ”£


 ½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ||
| ||
| c(CuCl 42- ) |
| c[Cu(H2O) 42- ]?c4(Cl-) |
| c(CuCl 42- ) |
| c[Cu(H2O) 42- ]?c4(Cl-) |
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ||
| ”÷ |
| ||
| ”÷ |
| 2016”Į6 |
| 2688”Į5 |
| 2016”Į6 |
| 2688”Į5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| 1 |
| 3 |
| 1 |
| 3 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 £Ø1£©×°Ņ©Ę·Ē°£¬Ó¦ĻČ½ųŠŠµÄ²Ł×÷
£Ø1£©×°Ņ©Ę·Ē°£¬Ó¦ĻČ½ųŠŠµÄ²Ł×÷| H2 | O2 | |
| ¢Ł | Zn”¢Ļ”ŃĪĖį | KClO3”¢MnO2 |
| ¢Ś | Zn”¢Ļ”ĮņĖį | H2O2ČÜŅŗ”¢MnO2 |
| ¢Ū | Zn”¢Ļ”ĻõĖį | KMnO4 |
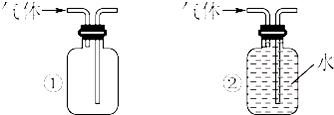
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com