
【题目】二价铬不稳定, 极易被氧气氧化。醋酸亚铬水合物{ [Cr(CH3COO)2]2·2H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水和醚,易溶于盐酸,是常用的氧气吸收剂。实验室中以锌粒、CrCl3溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如下图所示:
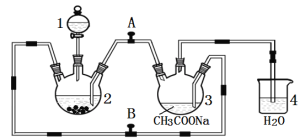
制备过程中发生的反应如下:
Zn(s) + 2HCl(aq) = ZnCl2(aq) + H2(g);
2CrCl3(aq) + Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
2Cr2+(aq) + 4CH3COO—(aq) + 2H2O(l) = [Cr(CH3COO)2]2·2H2O (s)
请回答下列问题:
(1)仪器1的名称是 , 所盛装的试剂是 。
(2)本实验中所用的溶液,配制用的蒸馏水都需事先煮沸,原因是 。
(3)实验开始生成H2气后, 为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应 阀门A、 阀门B (填“打开”或“关闭”)。
(4)本实验中锌粒须过量,其原因是 , 。
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质6.34 g,实验后得干燥纯净的[Cr(CH3COO)2]2·2H2O 5.64 g,请计算该实验所得产品的产率 。
(6)若使用该装置制备Fe(OH)2,且能较长时间看到Fe(OH)2白色沉淀现象。则在1、2、3中应装入的试剂依次为 、 、 。(写化学式)
【答案】(1)分液漏斗,盐酸与CrCl3溶液
(2)去除水中的溶解氧,防止Cr2+被氧化;
(3)打开;关闭
(4)与CrCl3充分反应得到CrCl2;产生足量的H2,(将装置中的空气排尽)将CrCl2溶液压入装置3与CH3COONa溶液反应(混合)
(5)75%;(6)H2SO4 ,Fe,NaOH ;
【解析】
试题分析:(1)根据仪器1的构造可知其名称为分液漏斗,盛装的稀盐酸与锌反应生成氢气,用来增大压强把生成的CrCl2溶液压入装置3中,故答案为:分液漏斗;盐酸与CrCl3溶液;
(2)由于二价铬不稳定,极易被氧气氧化,需要将配制用的蒸馏水事先煮沸,去除水中的溶解氧,防止Cr2+被氧化,故答案为:去除水中的溶解氧,防止Cr2+被氧化;
(3)实验开始生成H2气后,为使生成的CrCl2溶液与CH3COONa溶液顺利混合,打开A关闭B,把生成的CrCl2溶液压入装置3中反应,故答案为:打开;关闭;
(4)锌的作用是和盐酸反应生成氢气,增大仪器中的压强把生成的CrCl2溶液压入装置3,与CrCl3充分反应得到CrCl2,故答案为:与CrCl3充分反应得到CrCl2; 产生足量的H2,将CrCl2溶液压入装置3与CH3COONa溶液反应;
(5)实验时取用的CrCl3溶液中含溶质6.34g,理论上得到[Cr(CH3COO)2]22H2O 的质量为:![]() ×
×![]() ×376g/mol=7.52g,则该实验所得产品的产率为:
×376g/mol=7.52g,则该实验所得产品的产率为:![]() ×100%=75%,故答案为:75%;
×100%=75%,故答案为:75%;
(6)1和2中试剂制备亚铁盐,并用氢气排尽装置内空气,再将亚铁盐压入3中反应生成氢氧化亚铁,3中盛放氢氧化钠溶液,故答案为:H2SO4;Fe;NaOH。


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系 如图所示,下列说法中不正确的是( )

A.图中AB段的氧化剂为K2Cr2O7
B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C.开始加入的K2Cr2O7为0.25 mol
D.K2Cr2O7与FeSO4开始反应时物质的量之比为1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.离子键没有方向性和饱和性,而共价键有方向性和饱和性
B.离子键的强弱主要决定于离子半径和离子所带电荷数
C.配位键在形成时,由成键双方各提供一个电子形成一对共用电子
D.金属键的实质是金属中的自由电子与金属阳离子形成的一种强烈的相互作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的两随时间的变化曲线如图所示,据此回答:

(1)该反应的化学方程式为 。
(2)从开始至2min,Z的平均反应速率为 mol/(L·min);
(3)改变下列条件,可以加快化学反应速率的有_________
A.升高温度
B.减小物质X的物质的量
C.减小压强
D.增加物质Z的物质的量.
E.加入某种催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇与乙酸是生活中常见的两种有机物,试回答下列问题:
(1)乙醇中官能团的名称是__________,乙酸中官能团的结构简式为____________
(2)写出下列反应的化学方程式:
① 乙醇燃烧 _____________________________________________________
② 乙醇与Na _____________________________________________________
③ 乙酸与NaHCO3_____________________________________________________
④ 乙酸与CH3OH______________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:

已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用。
②ClO2气体在中性和碱性溶液中不能稳定存在。
(1)在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,请写出阳极的电极反应式 。
(2)反应生成ClO2气体需要X酸酸化,X酸可以为 。
A.盐酸 B.稀硫酸 C.硝酸 D.H2C2O4溶液
(3)吸收塔内的温度不能过高的原因为 。
(4)ClO2被S![]() 还原为ClO
还原为ClO![]() 、Cl
、Cl![]() 转化率与pH关系如图。写出pH≤2时ClO2与S
转化率与pH关系如图。写出pH≤2时ClO2与S![]() 反应的离子方程式: 。
反应的离子方程式: 。

(5)ClO2对污水中Fe2+、Mn2+、S2-和CN![]() 等有明显的去除效果。某工厂污水中含CN
等有明显的去除效果。某工厂污水中含CN![]() amg/L,现用ClO2将CN
amg/L,现用ClO2将CN![]() 氧化,生成了两种无毒无害的气体,其离子反应方程式为______________;处理100 m3这种污水,至少需要ClO2 _____________ mol。
氧化,生成了两种无毒无害的气体,其离子反应方程式为______________;处理100 m3这种污水,至少需要ClO2 _____________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知25℃时,Mg(OH)2的Ksp=1.8×l0-11,若要使0.18mol/L的MgCl2溶液生成Mg(OH)2沉淀,则至少需要将溶液的pH调至
A.5 B.5.5 C. 9 D.11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用铁矿石(主要成分为Fe2O3,还有SiO2、A12O3等杂质)提取Fe2O3。操作过程如下:

(1)(I)和(Ⅱ)步骤中分离溶液和沉淀的操作名称是 。
(2)写出Fe2O3和盐酸反应的离子方程式 。
(3)沉淀A中主要含有 。
(4)滤液Y中的阴离子除OH﹣、Cl﹣外,还有 (写离子符号)。
(5)过滤出氢氧化铁时需洗涤沉淀,洗涤沉淀的具体操作为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象中,是因为发生加成反应而产生的现象是
A. 乙烯使溴的四氯化碳溶液褪色
B. 将苯滴入溴水中,振荡后水层接近无色
C. 乙烯使酸性高锰酸钾溶液褪色
D. 甲烷与氯气混合,光照一段时间后黄绿色消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com