
 ��ش��������⣺
��ش��������⣺| Na2O2 |
| Al |
| �������� |
| Na2O2 |
| Al |
| �������� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��n��A��=n��C�� |
| B��n��B��=n��C�� |
| C��n��A��+n��B��=n��C�� |
| D��n��B��+n��C��=n��A�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij��ʳƷ�����ϱ�ǩ��ͼ��ʾ��
ij��ʳƷ�����ϱ�ǩ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
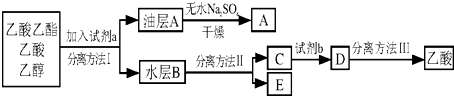
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ƿ�з��뼸�����Ƭ����ֹҺ�屩�� |
| B�����¶ȼ�ˮ�������������ƿ֧�ܿڸ��� |
| C����ˮ���������¿��룬�Ͽڳ� |
| D��������ƿ���õ�ʯ��������ֱ�Ӽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
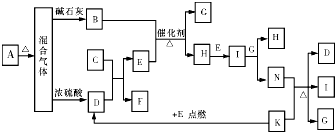 ��ͼ�е�B��K�ֱ�����йط�Ӧ��һ�ַ�Ӧ������������A��C��F��K�ǹ��壻E�dz��������嵥�ʣ�I�Ǻ���ɫ����̬�������̬����A���������Ⱥ����ɵ�����������ͨ����ʯ��ֻʣ������B����ͨ��Ũ������ֻʣ������D�������ʼ��ת����ϵ��ͼ��ʾ����ش��������⣺
��ͼ�е�B��K�ֱ�����йط�Ӧ��һ�ַ�Ӧ������������A��C��F��K�ǹ��壻E�dz��������嵥�ʣ�I�Ǻ���ɫ����̬�������̬����A���������Ⱥ����ɵ�����������ͨ����ʯ��ֻʣ������B����ͨ��Ũ������ֻʣ������D�������ʼ��ת����ϵ��ͼ��ʾ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HCHO ��ȩ |
| B��C6H5OH ���� |
| C��CH3Cl 1-�ȼ��� |
D��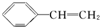 ����ϩ ����ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ʵ���Ũ����ȵĴ�����Һ������������Һ�������ϣ�c��Na+��+c��H+��=c��CH3COO-��+c��OH-��+c��CH3COOH�� |
| B��0.2mol/L NH4NO3��0.1 mol/L NaOH��Һ�������Ϻ�c��NH4+����c��NO3-����c��Na+����c��OH-����c��H+�� |
| C�������£�ͬŨ�ȵ�һԪ��HA��HB���룬����ͬŨ�ȵ�NaA��Һ��NaB��Һ��pH�� |
| D��ͬŨ�ȵ�������Һ����NH4Al��SO4��2����NH4Cl����NH3?H2O����CH3COONH4������c��NH4+���ɴ�С��˳���ǣ��٣��ڣ��ܣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���٢� | C���ڢ� | D���ڢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com