
| A£® | ŅŅ“¼ĘūÓĶŹĒŅ»ÖÖ“æ¾»Īļ | |
| B£® | ŅŅ“¼ĘūÓĶ×÷Č¼ĮĻ²»»į²śÉśĢ¼Ńõ»ÆĪļµČÓŠŗ¦ĘųĢ壬ĘäÓŵćŹĒæÉŅŌ¼õÉŁ¶Ō»·¾³µÄĪŪČ¾ | |
| C£® | ŅŅ“¼ŗĶĘūÓĶ¶¼æÉ×÷ČܼĮ£¬Ņ²æÉĻą»„Čܽā | |
| D£® | ŗĶŅŅ¶ž“¼»„ĪŖĶ¬ĻµĪļ |
·ÖĪö A”¢øł¾ŻŅŅ“¼ĘūÓĶµÄ×é³É³É·Ö£»
B”¢øł¾ŻŅŅ“¼ŗĶĘūÓĶµÄ×é³ÉŌŖĖŲ£¬æÉÖŖČ¼ÉÕ²śĪļÖŠŗ¬Ģ¼Ńõ»ÆĪļ£»
C”¢øł¾ŻŅŅ“¼ŗĶĘūÓĶµÄÓĆĶ¾ŗĶĪļĄķŠŌÖŹĄ“·ÖĪö£»
D”¢øł¾ŻĶ¬ĻµĪļµÄøÅÄī£ŗ½į¹¹ĻąĖĘ£¬·ūŗĻĶ¬Ņ»ĶØŹ½£¬ŌŚ×é³ÉÉĻĻą²īŅ»øö»ņnøöCH2£®
½ā“š ½ā£ŗA”¢ŅņŅŅ“¼ĘūÓĶµÄÖ÷ŅŖ³É·ÖĪŖŅŅ“¼ŗĶĘūÓĶ£¬ŹĒ»ģŗĻĪļ£¬¹ŹA“ķĪó£»
B”¢ŅņĘūÓĶµÄ×é³ÉŌŖĖŲ£ŗC”¢H”¢O£¬»¹ŗ¬ÓŠÉŁĮæµÄS£¬Č¼ÉÕ²śĪļÓŠĢ¼Ńõ»ÆĪļŗĶ¶žŃõ»ÆĮņ£¬ĘäÖŠ¶žŃõ»ÆĮņĪŪČ¾»·¾³£¬ŅŅ“¼µÄ×é³ÉŌŖĖŲ£ŗC”¢H”¢O£¬Č¼ÉÕ²śĪļÓŠĢ¼Ńõ»ÆĪļ£¬ĖłŅŌŅŅ“¼ĘūÓĶ×÷Č¼ĮĻČŌ»į²śÉśĢ¼Ńõ»ÆĪļµČÓŠŗ¦ĘųĢ壬µ«æÉŅŌ¼õÉŁ¶Ō»·¾³µÄĪŪČ¾£¬¹ŹB“ķĪó£»
C”¢ŅņŅŅ“¼ŗĶĘūÓĶ¶¼ŹĒ³£¼ūµÄÓŠ»śČܼĮĒŅÓŠ»śČܼĮÖ®¼äĶłĶłĻąČÜ£¬¹ŹCÕżČ·£»
D”¢ŅņĶ¬ĻµĪļŅŖĒó£ŗ½į¹¹ĻąĖĘ£¬·ūŗĻĶ¬Ņ»ĶØŹ½£¬ŌŚ×é³ÉÉĻĻą²īŅ»øö»ņnøöCH2£»¶ųŅŅ“¼ÖŠÓŠ1øöōĒ»ł£¬ŅŅ¶ž“¼ÖŠŗ¬ÓŠ2øöōĒ»ł£¬½į¹¹²»ĻąĻąĖĘ£¬¹ŹD“ķĪó£»
¹ŹŃ”£ŗC£®
µćĘĄ ±¾ĢāŠčŅŖĒæµ÷µÄŹĒĶ¬ĻµĪļµÄøÅÄī£¬½į¹¹ĻąĖĘ£¬ČōÓŠ¹ŁÄÜĶÅ£¬±ŲŠė¹ŁÄÜĶÅÖÖĄąŗĶŹżÄ涼ĻąĶ¬£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø Äæ±ź²āŹŌĻµĮŠ“š°ø
Äæ±ź²āŹŌĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
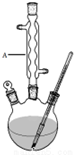 ¶¬ĒąÓĶÓÖ½ŠĖ®ŃīĖį¼×õ„£¬ŹĒŅ»ÖÖÖŲŅŖµÄÓŠ»śŗĻ³ÉŌĮĻ£®Ä³»ÆѧŠ”×éÓĆĖ®ŃīĖį£Ø
¶¬ĒąÓĶÓÖ½ŠĖ®ŃīĖį¼×õ„£¬ŹĒŅ»ÖÖÖŲŅŖµÄÓŠ»śŗĻ³ÉŌĮĻ£®Ä³»ÆѧŠ”×éÓĆĖ®ŃīĖį£Ø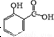 £©ŗĶ¼×“¼ŌŚĖįŠŌ“߻ƼĮ“ß»ÆĻĀŗĻ³ÉĖ®ŃīĖį¼×õ„²¢¼ĘĖćĘä²śĀŹ£®
£©ŗĶ¼×“¼ŌŚĖįŠŌ“߻ƼĮ“ß»ÆĻĀŗĻ³ÉĖ®ŃīĖį¼×õ„²¢¼ĘĖćĘä²śĀŹ£®| Ćū³Ę | ·Ö×ÓĮæ | ŃÕɫדĢ¬ | Ļą¶ŌĆÜ¶Č | ČŪµć£Ø”ę£© | ·Šµć£Ø”ę£© |
| Ė®ŃīĖį¼×õ„ | 152 | ĪŽÉ«ŅŗĢå | 1.18 | -8.6 | 224 |
| Ė®ŃīĖį | 138 | °×É«¾§Ģå | 1.44 | 158 | 210 |
| ¼×“¼ | 32 | ĪŽÉ«ŅŗĢå | 0.792 | -97 | 64.7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 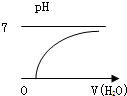 | B£® | 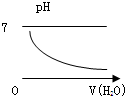 | C£® | 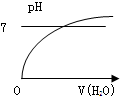 | D£® | 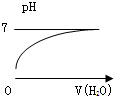 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ž | B£® | ¢Ł¢Ü¢Ž | C£® | ¢Ł¢Ż | D£® | ¢Ł¢Ż¢ß¢ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”°ĖÜĮĻĶõ”±¾ŪĖÄ·śŅŅĻ©ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ« | |
| B£® | ČżĀČ¼×Ķé£ØCHCl3£©æÉŅŌÓĆ¼×ĶéÓėĀČĘųµÄČ”“ś·“Ó¦Ą“ÖĘČ” | |
| C£® | ĖÄ·śŅŅĻ© £ØCF2=CF2£©ÖŠĖłÓŠµÄŌ×Ó¶¼ŌŚĶ¬Ņ»øöĘ½ĆęÉĻ | |
| D£® | ĖÄ·śŅŅĻ© £ØCF2=CF2£©Ķعż¼Ó¾Ū·“Ӧɜ³É”°ĖÜĮĻĶõ”±¾ŪĖÄ·śŅŅĻ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »Æѧ·“Ó¦·ÅČČŹĒŅņĪŖ·“Ó¦ĪļµÄ×ÜÄÜĮæµĶÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ | |
| B£® | ²»ŠčŅŖ¼ÓČČ¾ĶÄÜ·¢ÉśµÄ·“Ó¦ŹĒ·ÅČČ·“Ó¦ | |
| C£® | »ÆѧÄÜŹĒÄÜĮæµÄŅ»ÖÖŠĪŹ½£¬Ėü²»½öæÉŅŌ×Ŗ»ÆĪŖČČÄÜ£¬Ņ²ÄÜ×Ŗ»ÆĪŖµēÄÜ | |
| D£® | ĀČ»ÆÄĘ¾§ĢåČŪ»ÆŹ±£¬Ąė×Ó¼ü±»ĘĘ»µ£¬ĪüŹÕÄÜĮ棬·¢Éś»Æѧ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH3”śNO | B£® | HCl”śH2 | C£® | NaCl”śAgCl | D£® | Fe3+”śFe2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČÜŅŗµÄµ¼µēŠŌÓėČÜŅŗÖŠĄė×ÓµÄÅضČÓŠ¹Ų | |
| B£® | ČÜŅŗµÄµ¼µēŠŌÓėČÜŅŗÖŠĄė×ÓŹżÄæµÄ¶ąÉŁÓŠ¹Ų | |
| C£® | µĘÅŻ×ī°µŹ±ČÜŅŗÖŠĪŽ×ŌÓÉŅĘ¶ÆµÄĄė×Ó | |
| D£® | ĶłĒāŃõ»Æ±µČÜŅŗÖŠµĪ¼ÓŃĪĖįÓėµĪ¼ÓĮņĖįŹ±ĻÖĻóĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
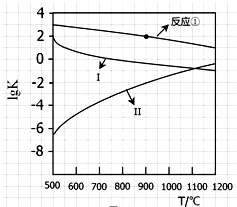 ÓĆCaSO4“śĢęO2ÓėČ¼ĮĻCO·“Ó¦£¬¼ČæÉĢįøßČ¼ÉÕŠ§ĀŹ£¬ÓÖÄܵƵ½øß“æCO2£¬ŹĒŅ»ÖÖøߊ§”¢Ēå½ą”¢¾¼ĆµÄŠĀŠĶČ¼ÉÕ¼¼Źõ£¬·“Ó¦¢ŁĪŖÖ÷·“Ó¦£¬·“Ó¦¢ŚŗĶ¢ŪĪŖø±·“Ó¦£®
ÓĆCaSO4“śĢęO2ÓėČ¼ĮĻCO·“Ó¦£¬¼ČæÉĢįøßČ¼ÉÕŠ§ĀŹ£¬ÓÖÄܵƵ½øß“æCO2£¬ŹĒŅ»ÖÖøߊ§”¢Ēå½ą”¢¾¼ĆµÄŠĀŠĶČ¼ÉÕ¼¼Źõ£¬·“Ó¦¢ŁĪŖÖ÷·“Ó¦£¬·“Ó¦¢ŚŗĶ¢ŪĪŖø±·“Ó¦£® £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com