
| A. | 工业合成氮属于人工固氮 | |
| B. | 含氮无机物和含氮有机物可以相互转化 | |
| C. | 氮的固定不一定是化学变化 | |
| D. | 碳、氢、氧三种元素也参与了氮循环 |
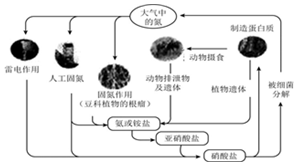
分析 A.人工固氮是人为的条件下将氮元素的单质转化为化合物的过程;
B.根据氮循环中物质的分类进行解答;
C.氮的固定是化学变化;
D.碳、氢、氧三种元素也参加了氮循环,如大气中的氮气转化氮的氧化物,氧元素参与,转化为铵盐,氢元素参加.
解答 解:A.工业合成氨是将N2与H2在一定条件下反应生成NH3,属于人工固氮,故A正确;
B.氮循环中铵盐和蛋白质可相互转化,铵盐属于无机物,蛋白质属于有机物,含氮无机物和含氮有机物可相互转化,故B正确;
C.氮的固定是将游离态的氮转化为化合化态,一定是化学变化,故C错误;
D.碳、氢、氧三种元素也参加了氮循环,如蛋白质的制造需要碳元素,又如N2在放电条件下与O2直接化合生成无色且不溶于水的一氧化氮气体,N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO,氧元素参与,二氧化氮易与水反应生成硝酸(HNO3)和一氧化氮,3NO2+H2O=2HNO3+NO,氢元素参加,故D正确.
故选C.
点评 本题主要考查了氮以及化合物的性质,主要是元素自然界中的循环图的理解应用,理解人工固氮、自然固氮的区别等知识点是解答的关键,题目难度不大.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 用碳棒连接电源的正极,另一电极用铜片 | |
| B. | 用铜片连接电源的正极,另一电极用铂片 | |
| C. | 阳极反应式为:Cu-2e═Cu2 | |
| D. | 阴极反应式为:2H++2e═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
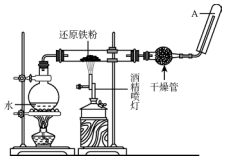 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验”.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验”.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2→H2SO4 | B. | SiO2→H2SiO3 | C. | Al2O3→Al(OH)3 | D. | Fe2O3→Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,5.6 L CCl4中含有的分子数目为0.25NA | |
| B. | 标准状况下,体积为22.4L的物质所含微粒数是NA | |
| C. | 常温常压下,0.5 mol NH3中含有的原子数目为2NA | |
| D. | 500mL1 mol•L-1 K2SO4溶液中含有的k+数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com