
分析 电离出的阳离子全部是氢离子的化合物为酸,而在水溶液中能完全电离的酸为强酸,只能部分电离的为弱酸;
电离出的阴离子全部是氢氧根的化合物为碱,在水溶液中能完全电离的碱为强碱,只能部分电离的为弱碱;
电离出的阳离子是金属离子或铵根离子、阴离子为酸根离子的化合物为盐,在水溶液中的溶解度大于1g的盐属于可溶性盐,溶解度小于0.1g的盐为难溶性盐.据此分析.
解答 解:(1)CH3COOH为酸,且由于不能完全电离,故为弱酸;
(2)H2SO4是酸,且由于能完全电离,故为强酸;
(3)Fe(OH)3 是碱,且由于部分电离,故为弱碱;
(4)CuSO4 是盐,且是可溶性盐;
(5)H2SO3 是酸,且由于不能完全电离,故为弱酸;
(6)NH3•H2O是碱,且由于不能完全电离,故为弱碱;
(7)KOH是碱,能完全电离,故为强碱;
(8)HNO3 是酸,且由于能完全电离,故为强酸;
(9)AgCl是盐,且由于溶解度小于0.1g,故为难溶性盐;
(10)Cu(OH)2 是碱,且由于不能完全电离,故为弱碱;
(ll)CaCO3 是盐,且由于溶解度小于0.1g,故为难溶性盐;
(12)H2CO3 是酸,且由于不能完全电离,故为弱酸;
(13)H2S 是酸,且由于不能完全电离,故为弱酸;
(14)NaOH 是碱,能完全电离,故为强碱;
(15)HCl 是酸,且由于能完全电离,故为强酸;
(16)KNO3 是盐,且是可溶性盐;
(17)NH4Cl 是盐,且是可溶性盐;
(18)NaHSO4 是盐,且是可溶性盐;
(19)NH4HCO3 是盐,且是可溶性盐;
(20)Cu2(OH)2CO3是盐,且由于溶解度小于0.1g,故为难溶性盐;
故答案为:(2)(8)(15);(7)(14);(1)(5)(12)(13);(3)(6)(10);(4)(16)(17)(18)(19);(9)(11)(20).
点评 本题考查了酸碱盐的概念以及酸碱性强弱的判断,并应注意酸碱性强弱和溶液中氢离子、氢氧根的浓度大小无必然关系,而取决于在水溶液中能否完全电离.


科目:高中化学 来源: 题型:实验题
 某化学小组设计如图装置,探究铜和一定量的浓HNO3是否反应是否有NO生成.已知:A试管内空气体积为50mL(标准状况),B广口瓶盛80mL水,硝酸不溶于煤油.
某化学小组设计如图装置,探究铜和一定量的浓HNO3是否反应是否有NO生成.已知:A试管内空气体积为50mL(标准状况),B广口瓶盛80mL水,硝酸不溶于煤油.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
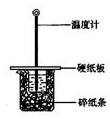 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:| 实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 试剂 | 试管中的物质 |  | |
| A | 苯环对甲基的影响 | 酸性KMnO4溶液 | ①苯②甲苯 | |
| B | 比较Br-、Fe2+和I-的还原性 | 氯水 | ①FeBr2溶液②FeI2溶液 | |
| C | 苯分子中没有碳碳双键 | Br2的CCl4溶液 | ①苯②己烯 | |
| D | 探究接触面积对反应速率的影响 | VmL、cmol/L的盐酸 | ①ag大理石块②ag大理石粉 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
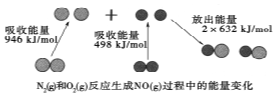 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是( )| A. | 1mol N2(g)和1mol O2(g)反应放出的能量为180kJ | |
| B. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 | |
| C. | 在1L的容器中发生反应,10min内 N2减少了1mol,因此10min内的平均反应速率为v(NO)=0.1mol/(L•min) | |
| D. | 1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 转移溶液后未洗涤烧杯和玻璃棒就直接定容 | |
| B. | 称量时左码右物 | |
| C. | 定容后把容量瓶倒转摇匀,发现液面低于刻度,再滴加几滴水至刻度线 | |
| D. | 在容量瓶中进行定容时俯视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸(HCOOH)与正丁醇 | B. | 乙酸与甲醇(CH3OH) | ||
| C. | 乙醇与CH3CH2COOH | D. | CH3CH2COOH与甲醇(CH3OH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com