

| A、装置①阳极有红色物质析出 |
| B、装置②的总反应为Cu+2Fe3+=Cu2++2Fe2+ |
| C、装置③中a为负极,发生的电极反应式为H2+2OH--2e-=2H2O |
| D、用装置④精炼铜,则a极为纯铜,电解质溶液可为CuSO4溶液 |


科目:高中化学 来源: 题型:
| A、NaCl |
| B、MgCl2 |
| C、KCl |
| D、CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸、纯碱、碳酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、光导纤维是以硅为主要原料制成的 |
| C、可依据是否有丁达尔现象区分溶液与胶体 |
| D、Fe(OH)3难溶于水,不存在氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
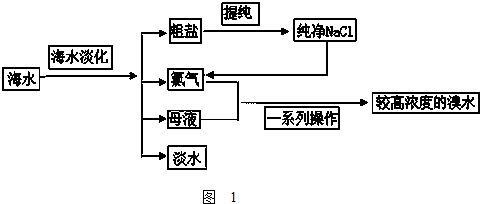

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、②③④ |
| C、①② | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电池总反应为:Mg+H2O2=Mg(OH)2 |
| B、正极发生的电极反应为:H2O2+2H++2e-=2H2O |
| C、工作时,正极周围海水的pH增大 |
| D、电池工作时,溶液中的H+向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
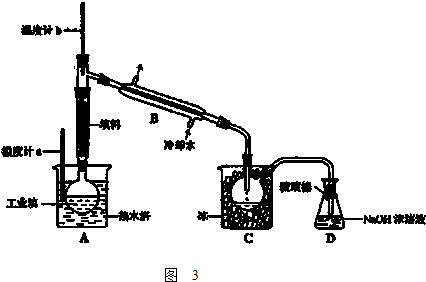
| 浸泡 |
| 过滤 |
| 氧化 |
| 萃取 |
| 分液 |
| 蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| △ |
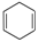 ,如果要合成
,如果要合成 ,所用的起始原料可以是( )
,所用的起始原料可以是( )| A、①④ | B、②③ | C、①③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com