
【题目】某同学按下列步骤配制500mL 0.200mol·L-1 Na2CO3溶液,请回答有关问题。
实验步骤 | 有关问题 |
(1)计算所需Na2CO3的质量 | 需要Na2CO3的质量为_________g。 |
(2)称量Na2CO3固体 | 称量过程中主要用到的仪器是_____ |
(3)将Na2CO3加入100mL烧杯中 | 为加快溶解速率,可采取的措施是___ |
(4)将烧杯中的溶液转移至500mL容量瓶中 | 为防止溶液溅出,应采取的措施是____________________________________________________________________________ |
(5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是______ |
(6)你认为按上述步骤配制的Na2CO3溶液的浓度是否为0.200mol·L-1,请说明理由。________
【答案】10.6g 托盘天平、药匙、烧杯 用玻璃棒搅拌 用玻璃棒引流,让烧杯中的溶液沿玻璃棒进入容量瓶中 直接加水至离刻度线1-2厘米处后,改用胶头滴管滴加至溶液凹液面与刻度线相平 不是,比0.200mol·L-1小,因为未洗涤烧杯,烧杯内壁上附着了一部分溶质,应该将烧杯洗涤2-3次,并将洗涤液一并转入容量瓶中。
【解析】
(1)依据n=cv,m=nM,计算m(Na2CO3);
(2)称量Na2CO3固体时,用到的仪器为:托盘天平、药匙、烧杯;
(3)固体溶解时,为加快溶解速度,可以用玻璃棒搅拌;
(4)向容量瓶中转移溶液时,应用玻璃棒引流;
(5)定容时,分两步,先加水至刻度1-2cm处,再改用胶头滴管加水;
(6)分析个不操作,找出可能引起的误差;
(1)配制500mL 0.200mol·L-1 Na2CO3溶液,需n(Na2CO3)=0.2mol/L![]() 0.5L=0.1mol,所以m(Na2CO3)=0.1mol
0.5L=0.1mol,所以m(Na2CO3)=0.1mol![]() 106g/mol=10.6g;
106g/mol=10.6g;
本题答案为:10.6g。
(2)称量Na2CO3固体时,用到的仪器为:托盘天平、药匙、烧杯;
本题答案为:托盘天平、药匙、烧杯
(3)Na2CO3加入100mL烧杯中,加水溶解,为加快溶解速率,用玻璃棒搅拌;
本题答案为:用玻璃棒搅拌。
(4)将烧杯中的溶液转移至容量瓶中时,用玻璃棒引流,让烧杯中的溶液沿玻璃棒进入容量瓶中;
本题答案为:用玻璃棒引流,让烧杯中的溶液沿玻璃棒进入容量瓶中。
(5)在容量瓶内的溶液定容时,先用烧杯直接加水至离刻度线1-2厘米处后,改用胶头滴管滴加至溶液凹液面与刻度线相平;
本题答案为:先用烧杯直接加水至离刻度线1-2厘米处后,改用胶头滴管滴加至溶液凹液面与刻度线相平。
(6)在转移时为洗涤烧杯,会导致所配溶液的浓度偏小,因为未洗涤烧杯,烧杯内壁上附着了一部分溶质,应该将烧杯洗涤2-3次,并将洗涤液一并转入容量瓶中。
本题答案为:不是,比0.200mol·L-1小,因为未洗涤烧杯,烧杯内壁上附着了一部分溶质,应该将烧杯洗涤2-3次,并将洗涤液一并转入容量瓶中。


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
①有大量的氯气泄漏时,应用浸有弱碱性溶液的毛巾捂住口鼻向低处跑
②钠在空气中加热,钠块先熔成光亮的银白色小球后燃烧
③Fe2O3可以做油漆的颜料
④用明矾做净水剂除去水中的悬浮物
⑤NaOH溶于水呈碱性,故可用于治疗胃酸过多
A.①③④B.②③④C.①②⑤D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)(题文)羟甲香豆素是一种治疗胆结石的药物,合成路线如下图所示:
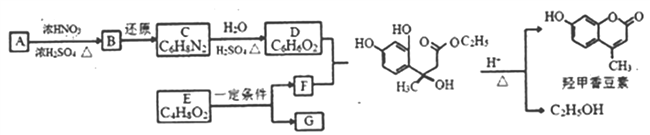 己知:(1)
己知:(1)![]()
(2)2CH3COOCH3 ![]() CH3COCH2COOCH3+CH3OH
CH3COCH2COOCH3+CH3OH
(3)RCOOR'+R"OH ![]() RCOOR"+ R'OH(R、R'、R"代表烃基)
RCOOR"+ R'OH(R、R'、R"代表烃基)
(4)有机物G的红外光谱和核磁共振氢谱如下图所示
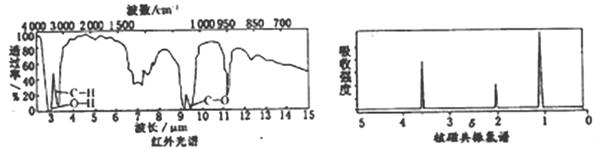
回答下列问题:
(1)A→B的反应类型___________,D的名称为_________________。
(2)C分子中可能共平面的最多原子数目是__________;E中含氧官能团名称____________。
(3)2E→F+G,化学方程式为______________________________。
(4)H为物质F的同分异构体,能发生水解反应,且0.1molH与银氨溶液发生反应后生成43.2g银。符合上述条件的共有_____种。
(5)以CH3COOCH3和苯酚为原料,制备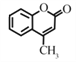 的合成路线(其他试剂任选) _____
的合成路线(其他试剂任选) _____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应发生在同种元素之间的是( )
A. Zn+2HCl![]() ZnCl2+H2↑
ZnCl2+H2↑
B. 2H2S+SO2![]() 3S↓+2H2O
3S↓+2H2O
C. H2+CuO![]() Cu+H2O
Cu+H2O
D. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
|
|
|
|
A.甲醇低温所制氢气用于新能源汽车 | B.氘、氚用作“人造太阳”核聚变燃料 | C.偏二甲肼用作发射“天宫二号”的火箭燃料 | D.开采可燃冰,将其作为能源使用 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。其结构片段如下图

下列关于该高分子的说法正确的是
A. 完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境
B. 完全水解产物的单个分子中,含有官能团―COOH或―NH2
C. 氢键对该高分子的性能没有影响
D. 结构简式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,摩托罗拉公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。某兴趣小组用右图模拟该电池工作原理。已知甲池的总反应式为:2CH3OH+3O2+4KOH![]() 2K2CO3+6H2O。请填空:
2K2CO3+6H2O。请填空:
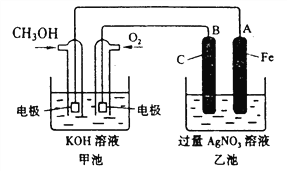
(1)充电时:①原电池的负极与电源_______极相连。
②阳极的电极反应式为____________________________________________。
(2)放电时:负极的电极反应式为_______________________________________________。
(3)某兴趣小组的同学用如图装置进行如下实验:在此过程中若完全反应,乙池中A极的质量升高648g,则甲池中理论上消耗O2 的体积为________L(标准状况下)。
(4)已知常温时CuS的Ksp=1.3×10-36,向100 mL 2×10-18 mol·L-1的K2S溶液中加入100 mL 2×10-18 mol·L-1的CuCl2溶液,试通过计算说明有无CuS沉淀生成(写出计算推理过程,忽略溶液混合时的体积变化)_____________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组通过测量溶液的电导率(电导率越大,说明溶液的导电能力越强)探究沉淀溶解平衡,各物质的电导率数据如下:
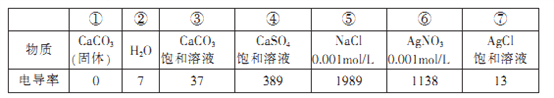
下列分析不正确的是
A. CaCO3固体中不存在白由移动的离子
B. 与②对比,说明⑦中存在:AgCl=Ag++ Cl-
C. ⑤、⑥等体积混合后过滤,推测滤液的电导率一定大于13
D. 将①中固体加入④中,发生反应:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是自然界碳循环中的重要物质。下列过程会引起大气中CO2含量上升的是
A. 光合作用 B. 自然降雨
C. 化石燃料的燃烧 D. 碳酸盐的沉积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com