
| A. | Na2CO3溶液的浓度为0.2mol•L-1 | |
| B. | 当V(盐酸)=0时,溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | |
| C. | 当V(盐酸)=25.00mL时,溶液中:c(Cl-)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 当V(盐酸)=50.00mL时,溶液中:c(Na+)+c(H+)=c(OH-)+c(Cl-) |
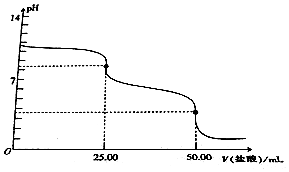
分析 A.用0.1mol•L-1的盐酸滴定25.00mLNa2CO3溶液,当消耗V(HCl)=25.00mL时,溶液的pH发生急剧变化,说明此时二者恰好完全反应,二者物质的量以1:1反应;
B.当盐酸体积为0时,溶液中溶质为碳酸钠,存在质子守恒,根据质子守恒判断;
C.当V(盐酸)=25.00mL时,溶液中溶质为等物质的量浓度的碳酸氢钠和氯化钠,碳酸氢根离子水解导致溶液呈碱性,但其水解程度较小,其水解程度大于电离程度;
D.当V(盐酸)=50.00mL时,二者恰好完全反应生成氯化钠、碳酸,溶液中存在电荷守恒,根据电荷守恒判断.
解答 解:A.用0.1mol•L-1的盐酸滴定25.00mLNa2CO3溶液,当消耗V(HCl)=25.00mL时,溶液的pH发生急剧变化,说明此时二者恰好完全反应,二者物质的量以1:1反应,二者的体积相,则浓度相等,所以碳酸钠溶液浓度为0.1mol/L,故A错误;
B.当盐酸体积为0时,溶液中溶质为碳酸钠,存在质子守恒,根据质子守恒得c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3),故B正确;
C.当V(盐酸)=25.00mL时,溶液中溶质为等物质的量浓度的碳酸氢钠和氯化钠,碳酸氢根离子水解导致溶液呈碱性,但其水解程度较小,其水解程度大于电离程度,所以c(CO32-)<c(H2CO3),故C错误;
D.当V(盐酸)=50.00mL时,二者恰好完全反应生成氯化钠、碳酸,溶液中存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(Cl-)+(HCO3-)+2c(CO32-),故D错误;
故选B.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断能力,明确图象中每个点溶液中溶质成分及其性质是解本题关键,注意电荷守恒和物料守恒的灵活运用,易错选项是D.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.01 mol•L-1HA的溶液中 c(H+)=l×l0-4mol•L-1 | |
| B. | pH=3的HA溶液与pH=ll的NaOH溶液等体积混合后所得溶液中:c(Na+)=c(A-)>c(OH-)=c(H+) | |
| C. | 浓度均为0.1 mol•L-1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(H+)-c(OH-)>c(A-)-c(HA) | |
| D. | pH=3的HA溶液与pH=11的NaOH溶液混合后所得溶液显碱性,则 c(Na+)>c(A-)>c(OH-)><c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 在试管中加入少量FeCl3溶液和过量 (填少量、过量)的KI溶液. | 深红色如期出现 |
| ② | 将试管中的混合溶液转移至分液漏斗 (填仪器)中,倒入一定量的CCl4, 塞住活塞,充分振荡(萃取),静置. | 液体分层,上层接近无色,下层紫红色 |
| ③ | 打开活塞,先放出下层液体,再从分液漏斗的上口中倒出水层于试管中,加入KSCN溶液 | 出现血红色,则反应后的混合物中含Fe3+,进而证明这的确是一个可逆反应;反之则不含Fe3+,进而证明不是一个可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

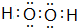 ,化合物E2 D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为Na2O2+2H2O+S2-=S+4Na++4OH-
,化合物E2 D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为Na2O2+2H2O+S2-=S+4Na++4OH-查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钡与盐酸反应 2H++BaCO3=Ba2++H2O+CO2↑ | |
| B. | 氢氧化钡溶液与稀硫酸混合 Ba2++SO42-+H++OH-=BaSO4↓+H2O | |
| C. | 氯气通入蒸馏水中 Cl2+H2O=Cl-+ClO-+2 H+ | |
| D. | CO2通入过量的澄清石灰水中 CO2+Ca(OH)2=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向海水中加入明矾可以使海水淡化,用于解决淡水供应危机 | |
| B. | 大力推广农作物的生物防治技术,以减少农药的使用 | |
| C. | 将地沟油回收再加工为食用油,以减缓水体富营养化 | |
| D. | 用聚氯乙烯代替木材,生产包装盒、快餐盒等,以减少木材的使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若生成物C、D中有一种为单质,则该反应一定是置换反应 | |
| B. | 若生成物C和D分别为两种沉淀,A、B有可能为盐和碱 | |
| C. | 若C、D是盐和水,则A、B一定是酸和碱 | |
| D. | 若C、D是两种化合物,则A、B一定是化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、OH-、Al3+、Cl- | B. | K+、SO42-、HCO3-、Na+ | ||
| C. | Mg2+、NO3-、Cl-、Na+ | D. | MnO4-、K+、SO42-、Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com