
【题目】控制变量是科学研究的重要方法。相同质量的铁粉与足量稀硫酸分别在下列条件下发生反应,其中反应速率最快的是
A | B | C | D | |
t/℃ | 10 | 10 | 40 | 40 |
c(H2SO4 )/(mol/L) | 1 | 3 | 1 | 3 |
A. AB. BC. CD. D
科目:高中化学 来源: 题型:
【题目】下列对生活中有关化学问题的分析正确的是( )
A.钙和磷都是人体内含量丰富的矿物元素,它们都属于微量元素
B.垃圾焚烧和发电技术的结合,既解决了污染问题,又有效利用了垃圾所含的能量
C.制造普通玻璃的主要反应原理之一为:CaO+SiO2 ![]() CaSiO3
CaSiO3
D.青霉素是最早发现的天然抗生素,其中起治疗作用的是水杨酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法不正确的是( ) 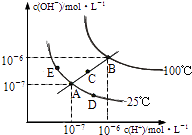
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到D点,可采用:温度不变在水中加入少量的酸
C.若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体
D.若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
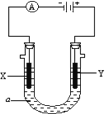
(1)若要在铁制品表面镀上一层银,则
①X电极的材料是____,电极反应式____________
②Y电极反应式__________________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极反应式_______________
②Y电极的材料是_______,电极反应式___________________(杂质发生的反应不必写出).
③假若电路中有0.04摩尔电子通过时,阴极增重________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝镁合金材料在现代装饰材料中占有极为重要的地位,这种材料常用于制作门窗框、防护栏等。下列铝镁合金的性质与这些用途无关的是
A.不易生锈B.导电性好C.密度小D.强度高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于生物体内化合物的说法不正确的是( )
A. 脂肪是既能贮能又具有保温作用的物质
B. 蛋白质是控制细胞生命活动的大分子
C. 无机盐离子可以维持内环境的渗透压
D. 核酸承担了遗传信息贮存和传递的任务
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铅[2PbCO3Pb(OH)2]是生产铅酸蓄电池正极的原料.
(1)某研究小组制备碱式碳酸铅的主要实验流程如图: 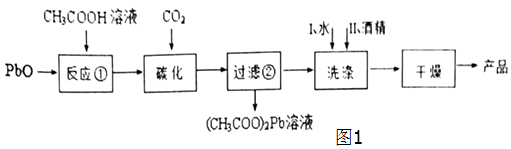 ①“反应①”的生成物是(CH3COO)2PbPb(OH)2 , 该反应是在90℃、搅拌并保温3h的条件下完成的,则该反应的化学方程式为
①“反应①”的生成物是(CH3COO)2PbPb(OH)2 , 该反应是在90℃、搅拌并保温3h的条件下完成的,则该反应的化学方程式为
②过滤时所志要的玻璃仪器有漏斗
③沉淀经水洗涤后又用洒精洗涤的目的是
(2)为确定2PbCO3Pb(OH)2的热分解过程,进行了如下实验: 称取一定量(1)中制得的产品放在热重分析仪中,在氩气流中加热分解,测得残留固体的质量随温度的变化如图所示.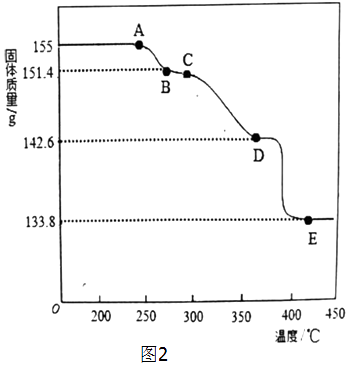
①A→B过程中,逸出的分解产物的化学式为;E点残留固体的化学式为
②根据图中数据,计算并确定D点残留固体的化学式(写出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CO合成甲醇(CH3OH)的化学反应方程式为: CO(g)+2H2(g)CH3OH(g)△H<0按照相同的物质的量投料,测的CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
A.平衡常数:K(a)>K(c),K(b)=K(d)
B.正反应速率:v(a)>v(c),v(b)>v(d)
C.平均摩尔质量:M(a)<M(c),M(b)>M(d)
D.平衡时a点一定有n(CO):n(H2)=1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com