
| A. | X2+>R2+>Y2+>Z2+ | B. | Y2+>Z2+>R2+>X2+ | C. | Z2+>X2+>R2+>Y2+ | D. | R2+>X2+>Z2+>Y2+ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
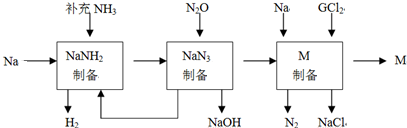
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②⑤ | C. | ④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气具有还原性,可用于检查HCl泄漏 | |
| B. | 浓硫酸具有脱水性,可用于干燥CO2 | |
| C. | 氧化铝具有高熔点,可用于生产耐火砖 | |
| D. | Cl2有酸性,可与烧碱反应制备含氯消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 活化分子具有的能量就是活化能 | |
| B. | 增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大 | |
| C. | 无论是吸热反应还是放热反应,升高温度都能增大活化分子百分数 | |
| D. | 活化分子间的碰撞一定是有效碰撞 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向AgCl悬浊液中加入KI溶液:AgCl(s)+I-(aq)═AgI(s)+Cl-(aq) | |
| B. | 明矾净水:Al3++3H2O?Al(OH)3+3H+ | |
| C. | 90℃时,测得纯水中Kw=3.8×10-13:H2O(l)?H+(aq)+OH-(aq)△H<0 | |
| D. | 用热的纯碱溶液可以清洗油污:CO32-+H2O?HCO3-+OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com