
����Ŀ������������(NOx)�Ǵ�����Ⱦ��֮һ����ҵ����һ���¶Ⱥʹ�����������NH3��NOx��ԭ����N2��ijͬѧ��ʵ�����ж�NH3��NOx��Ӧ������̽�����ش��������⣺
��1���������Ʊ�

�������ķ���װ�ÿ���ѡ����ͼ�е�_________����Ӧ�Ļ�ѧ����ʽΪ_______________��
�����ռ�һƿ����İ�����ѡ����ͼ�е�װ�ã�������˳��Ϊ������װ����______(������������Сд��ĸ��ʾ)��
��2����������������ķ�Ӧ
�������ռ�����NH3����ע����X�У�Ӳ�ʲ�����Y�м�����������������NO2(�����ü���K1��K2�к�)����һ���¶��°�ͼʾװ�ý���ʵ�顣

�������� | ʵ������ | ����ԭ�� |
��K1���ƶ�ע����������ʹX�е����建��ͨ��Y���� | ��Y����_____________ | ����Ӧ�Ļ�ѧ����ʽ ____________ |
��ע���������˻�ԭ�����̶�����װ�ûָ������� | Y����������ˮ�� | ���ɵ���̬ˮ���� |
��K2 | ��_______________ | ��______________ |
���𰸡���1���� A�� 2NH4Cl+Ca(OH)2![]() 2NH3��+ CaCl2+2H2O(��B��NH3��H2O
2NH3��+ CaCl2+2H2O(��B��NH3��H2O![]() NH3��+H2O)��
NH3��+H2O)��
��d c f e i��
��2��������ɫ����������dz����8NH3+6NO2 ![]() 7N2 +12H2O��
7N2 +12H2O��
��Z��NaOH��Һ������������������Ӧ������������������Y����ѹǿС����ѹ��
��������
�����������1������ʵ�����У���������������NH4Cl��ϼ����������ֽⷴӦ��ȡ����������������NH4Cl���ǹ��壬�������������ȡ���壬��Ӧѡ��Aװ����������ȡ������������Ӧ�Ļ�ѧ����ʽΪ2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O��Ҳ��������NH3��H2O�IJ��ȶ��ԣ����������ȷֽ����������ˮ��ȡ��������ʱӦ��ѡ���װ����װ��B����Ӧ�Ļ�ѧ����ʽ�ǣ�NH3��H2O
CaCl2+2NH3��+2H2O��Ҳ��������NH3��H2O�IJ��ȶ��ԣ����������ȷֽ����������ˮ��ȡ��������ʱӦ��ѡ���װ����װ��B����Ӧ�Ļ�ѧ����ʽ�ǣ�NH3��H2O![]() NH3��+H2O��������A(��B)װ���Ƶõİ��������ڰ����Ǽ������壬������Ҫ�������Ը������ʯ�ҽ��и��Ȼ���ٸ��ݰ������ܶȱȿ���С�����ʣ��������ſ������ռ��������Ǵ�����Ⱦ�Ҫ����β������������������ˮ�м����ܽ�����������ˮ�����ռ�����β����������װ�õ�����˳��Ϊd��c��f��e��i����2����NO2����ǿ�����ԣ�NH3��ǿ��ԭ�ԣ������������ᷢ��������ԭ��Ӧ����������ˮ�����ݵ����غ㡢ԭ���غ㣬�ɵ÷�Ӧ�ķ���ʽ��8NH3+6NO2
NH3��+H2O��������A(��B)װ���Ƶõİ��������ڰ����Ǽ������壬������Ҫ�������Ը������ʯ�ҽ��и��Ȼ���ٸ��ݰ������ܶȱȿ���С�����ʣ��������ſ������ռ��������Ǵ�����Ⱦ�Ҫ����β������������������ˮ�м����ܽ�����������ˮ�����ռ�����β����������װ�õ�����˳��Ϊd��c��f��e��i����2����NO2����ǿ�����ԣ�NH3��ǿ��ԭ�ԣ������������ᷢ��������ԭ��Ӧ����������ˮ�����ݵ����غ㡢ԭ���غ㣬�ɵ÷�Ӧ�ķ���ʽ��8NH3+6NO2![]() 7N2 +12H2O�����ݷ�Ӧ����ʽ��֪��Ӧ�����ǣ�Y���ڿ�������ɫ����������dz��ͬʱ��ע�������ڱ���ˮ���������������������֪�����÷�Ӧ�ķ���ʽ��8NH3+6NO2
7N2 +12H2O�����ݷ�Ӧ����ʽ��֪��Ӧ�����ǣ�Y���ڿ�������ɫ����������dz��ͬʱ��ע�������ڱ���ˮ���������������������֪�����÷�Ӧ�ķ���ʽ��8NH3+6NO2![]() 7N2 +12H2O������Ӧ��������������������ʵ������٣����Ի�ʹ����������ѹǿ��С������K2���ձ���NaOH��Һ�ڴ���ѹǿ�������»ᵹ������Y���ڣ�����Һ����Y���ڵ�ԭ���������÷�Ӧ�����������С�ķ�Ӧ����Ӧ��������װ����ѹǿ���ͣ����������ѹ�������¶�������������
7N2 +12H2O������Ӧ��������������������ʵ������٣����Ի�ʹ����������ѹǿ��С������K2���ձ���NaOH��Һ�ڴ���ѹǿ�������»ᵹ������Y���ڣ�����Һ����Y���ڵ�ԭ���������÷�Ӧ�����������С�ķ�Ӧ����Ӧ��������װ����ѹǿ���ͣ����������ѹ�������¶�������������


 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС������ͼװ�ý���SO2��FeCl3��Һ��Ӧ�����ʵ��(�г�װ������ȥ)��
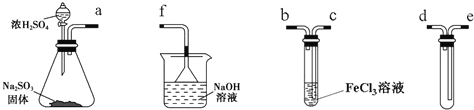
��1����װ����������������ȷ������˳����a��______��______��______��______��______��
��2���ձ��е���©����������_______________________��
��3����FeCl3��Һ��ͨ������SO2ʱ���۲쵽������Ϊ__________________��
��4��������������С��ͬѧ��ΪSO2��FeCl3��Һ������������ԭ��Ӧ��
��д��SO2��FeCl3��Һ��Ӧ�����ӷ���ʽ__________________��
����С��ͬѧ��ʢװFeCl3�Թܷ�Ӧ�����Һ�м��������ữ��BaCl2��Һ�������ְ�ɫ����������֤����Ӧ������SO42-����������������������__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ԭ�������ĵ��������ֶ�����Ԫ��(����ĸx�ȱ�ʾ)ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯��ͼ��ʾ�������жϳ���Ԫ�ػش����⣺
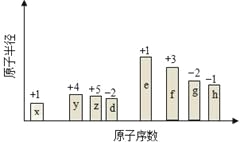
��1��f��Ԫ�����ڱ���λ����____________________________��
��2���Ƚ�d��e�������ӵİ뾶��С______��______���û�ѧʽ��ʾ����ͬ�����Ƚ�g��h������������Ӧ��ˮ���������ǿ��___________��____________��
��3����ѡ����Ԫ�����һ����ԭ�ӹ��ۻ����д�������ʽ______________________��
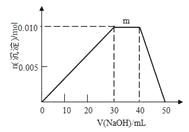
��4������Ԫ�ؿ������R��zx4f(gd4)2����ʢ��10 mL 1 mol��L-1 R��Һ���ձ��еμ�1 mol��L-1 NaOH��Һ���������ʵ�����NaOH��Һ����仯��ͼ��ʾ��
�� д��m�η�Ӧ�����ӷ���ʽ_______________________________��
�� ����R��Һ�иļ�20 mL 1.2 mol��L-1Ba(OH)2��Һ����ַ�Ӧ����Һ�в������������ʵ���Ϊ___________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Դ�����þ��й���ǰ����
��1����ͼ�ǴӺ�ˮ����ȡþ�ļ����̣�
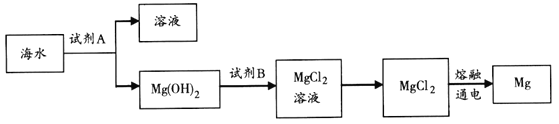
�ٹ�ҵ�ϳ����ڳ���Mg2+���Լ�A��________��Mg(OH)2ת��ΪMgCl2�����ӷ���ʽ��_______��
������ˮMgCl2��ȡMg�Ļ�ѧ����ʽ��________��
��2���������и�����I����ʽ���ڵĵ�Ԫ�أ�ʵ������ȡI2��;��������ʾ��
![]()
�����պ������ҽ�ʱ���õ���Ҫ����������________��
�����ữ����Һ�мӹ���������Һ��д���÷�Ӧ�����ӷ���ʽ________��
�۷�Ӧ��������CCl4����ȡ����������ȡ����Һ�ķ����ӵ�ˮ����ȡ�⣬��Ҫ����������ͼ��
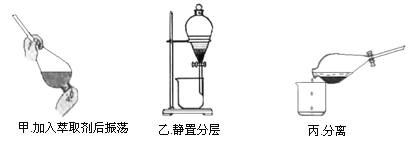
�ס��ҡ���3��ʵ������У�����ȷ����________����ס������ҡ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������̿�(MnCO3)�ۺ�FeCO3��SiO2��Cu2(OH) 2CO3�����ʣ�Ϊԭ����ȡ�������̣�������ʾ��ͼ���£�
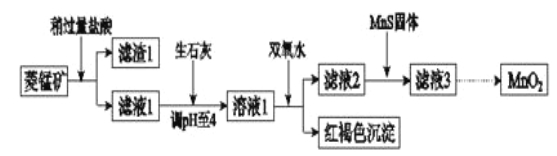
��֪�������������������pH
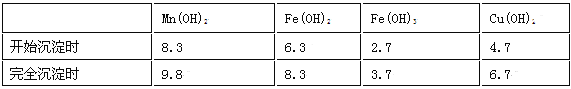
ע���������ӵ���ʼŨ��Ϊ0.1 mol/L,�ش��������⣺
��1�������ʵ����̿�ʹ��ǰ�轫����飬��ҪĿ���� _______ ___________ �������ܽ�MnCO3�Ļ�ѧ����ʽ��_______ ______________ ___ _____��
��2������Һ1�м���˫��ˮʱ����Ӧ�����ӷ���ʽ�� _______ ___________ ��
��3����Һ2�м����Թ��������ܵ����MnS���Գ�ȥCu2+����Ӧ�����ӷ���ʽ�� ________ ��
��4����MnCl2ת��ΪMnO2��һ�ַ���������������������������ữ��NaClO3��Һ��MnCl2�������÷�Ӧ�����ӷ���ʽΪ����Mn2������ClO3������________����________����________����________��
��5����MnCl2ת��ΪMnO2����һ�ַ����ǵ�ⷨ��
�� ��������MnO2�ĵ缫��Ӧʽ�� ____ ___ ____________ _______ ��
����ֱ�ӵ��MnCl2��Һ������MnO2��ͬʱ���������Cl2������Cl2�IJ����� _____ ��
����������MnCl2��Һ�м���һ������Mn(NO3)2��ĩ������Cl2��������ԭ���� ___ __ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��2����ѧ�뼼��]������أ�KMnO4����һ�ֳ�������������Ҫ���ڻ�������������ҩ��ҵ�ȡ������̿���Ҫ�ɷ�ΪMnO2��Ϊԭ������������صĹ���·�����£�

�ش��������⣺
��1��ԭ�����̿����������ذ�1��1�ı��������泴�����л��䣬����ǰӦ�����̿���飬�������� ��
��2����ƽ¯���з����Ļ�ѧ����ʽΪ ��
��3����ƽ¯������Ҫ��ѹ����Ŀ���� ��
��4����K2MnO4ת��ΪKMnO4�����������ֹ��ա�
����![]() �绯�����Ǵ�ͳ���գ�����K2MnO4��Һ��ͨ��CO2���壬ʹ��ϵ�����Ի������ԣ�K2MnO4�����绯��Ӧ����Ӧ������K2MnO4��MnO2�� ��д��ѧʽ����
�绯�����Ǵ�ͳ���գ�����K2MnO4��Һ��ͨ��CO2���壬ʹ��ϵ�����Ի������ԣ�K2MnO4�����绯��Ӧ����Ӧ������K2MnO4��MnO2�� ��д��ѧʽ����
�ڡ���ⷨ��Ϊ�ִ����գ������K2MnO4ˮ��Һ�����������������ĵ缫��ӦΪ �������ݳ��������� ��
������ⷨ������![]() �绯�����У�K2MnO4������������֮��Ϊ ��
�绯�����У�K2MnO4������������֮��Ϊ ��
��5��������ش��ȵIJⶨ����ȡ1.0800 g��Ʒ���ܽ������100 mL����ƿ�У�ҡ�ȡ�ȡŨ��Ϊ0.2000 mol��L1��H2C2O4����Һ20.00 mL������ϡ�����ữ����KMnO4��Һƽ�еζ����Σ�ƽ�����ĵ����Ϊ24.48 mL������Ʒ�Ĵ���Ϊ ���г�����ʽ���ɣ���֪2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪X��Y��Z��W����Ԫ����Ԫ�����ڱ�������������ͬ�����ڵ�Ԫ�أ���ԭ��������������X��Wͬ���壬Y��ZΪͬ���ڵ�����Ԫ�ء�Wԭ�ӵ�����������Y��Zԭ������������֮�͡�Y���⻯���������3�����ۼ���Zԭ�������������Ǵ�����������3�������ƶϣ�
��1��X��Y��Z��W����Ԫ�صķ��ţ�
X___________��Y___________��Z___________��W___________��
��2��������Ԫ���е�����Ԫ����ɵ�������ˮ��ˮ��Һ�Լ��ԵĻ�����ĵ���ʽ�ֱ�
Ϊ_____________��___________________��
��3����X��Y��Z���γɵ����ӻ�������_____________�����ѧʽ������W������������ˮ�����Ũ��Һ����ʱ�����ӷ���ʽ��____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼͭпԭ���ʾ��ͼ���ش��������⣺
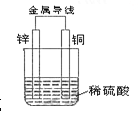
��1����ԭ��������ӷ�Ӧʽ�� ��
��2�����·�����ķ����Ǵ� (��Zn��Cu��Cu��Zn)��
��3���ڵ�صĹ��������У�Zn�������仯��3.25g����Cu������ (����ӡ��������䡱���١�)����·��ת�Ƶ���Ϊ mol��ͭ�������������� L(��״����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Zn��Cu��������Һ��ɵ�ԭ��أ�����һ��ʱ���пƬ������������6.5 g���ش��������⣺
��1������ԭ��ص������ǣ�___________�������ĵ缫��Ӧʽ��__________________________________��
��2�������������Һ��Ϊ����ͭ��Һ�������ǣ�________�������ĵ缫��Ӧʽ��_________________������������ͬ�ĵ���ʱ�����������������Ϊ______________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com