
【题目】在化学反应X+2Y→R+2M 中,已知R和M的摩尔质量之比为22:9,当1.6克X与Y恰好完全反应后,生成4.4克R,则Y与M的质量依次为_____________,解答此题时使用到的化学定律是_____________.
科目:高中化学 来源: 题型:
【题目】短周期非金属元素X和Y能形成XY2型化合物,下列有关说法正确的是
A.XY2一定能与水反应B.X可能是ⅣA、VA或ⅥA族元素
C.符合要求的XY2物质有两种D.X、Y一定不是同一主族的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾(K2Cr2O7)是高中化学常见的的氧化剂,工业上以铬铁矿为原料用碱溶氧化法制备。铬铁矿中通常含有Cr2O3、FeO、Al2O3、SiO2等。
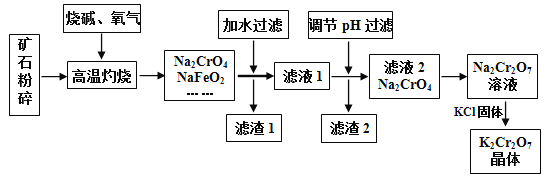
已知:
①NaFeO2常温遇大量水会强烈水解,高温时不与水反应
②2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
③+6价的铬元素在强酸性条件下具有强氧化性,还原产物为Cr3+,强碱性条件下几乎没有氧化性;请回答下列问题:
(1)将矿石粉碎的目的是___________________________。
(2)高温灼烧时生成NaFeO2的化学方程式____________________________________。
(3)①滤渣1中有红褐色物质,滤渣1的成分为__________________(写化学式,下同),写出生成该物质反应的离子方程式___________________________。
②滤渣2的主要成分是__________________。
(4)若向Na2CrO4溶液中加入浓盐酸进行酸化,出现的现象为__________________
(5)生产后的废水中主要含有一定量的Cr2O72-,通常加一定量的绿矾进行净化并调节pH约为6,可生成两种难溶于水的沉淀,请写出该反应的离子方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题。
(1)利用VSEPR推断分子或离子的空间构型:![]() ___________;SeO3__________。
___________;SeO3__________。
(2)与SeO3互为等电子体的一种离子为_____(填化学式)。SCN-电子式_______。
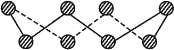
(3)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是__。
(4)硒、溴与砷同周期,三种元素的第一电离能从大到小顺序为__________(用元素符号比较)。
(5) 已知常温下Ni(CO)4是无色液体,其构型为正四面体。则配位原子是______,晶体类型为__________,推测其______(填“难”或“易”)溶于水。
(6)CO2晶胞中,与CO2紧邻的CO2有_______个。
(7)酸性比较:H2SeO3______H2SeO4 ,原因_________________________________。
(8)向CuSO4溶液中滴加氨水,溶液先出现沉淀后沉淀溶解,写出沉淀溶解的离子方程式_____________________________,[Cu(H2O)4]2+易转化为[Cu(NH3)4]2+原因__________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国明代《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次价值倍也”。这里用到的实验方法可用于分离
A. CCl4和水 B. 酒精和水 C. 食盐水和泥沙 D. 硝酸钾和硫酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C.J.Pedersen教授由于合成了冠醚而获得诺贝尔奖。这类醚因形似“王冠”故称冠醚。如
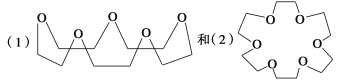
下列关于冠醚的说法正确的是
A. 冠醚属于烃类
B. (2)式与葡萄糖互为同分异构体
C. 冠醚能燃烧生成 CO2和H2O
D. (1)式和(2)式互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)科学家发现某药物M能治疗血管疾病,是因为它在人体内能释放出一种“信使分子”D,已知M的相对分子质量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%,则M的分子式是________________。D是双原子分子,相对分子质量为30,则D的分子式为________________。
(2)油脂A经下列途径可得到M:
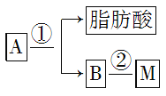
图中②的提示:R—OH+HO—NO2![]() R—O—NO2+H2O(R代表烃基),反应②的化学方程式为___________________________________。
R—O—NO2+H2O(R代表烃基),反应②的化学方程式为___________________________________。
(3)C是B和乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式___________________________________。
(4)若将0.1 mol B与足量的金属钠反应,则需消耗________ g金属钠。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。
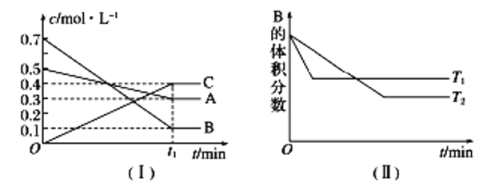
根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为________,正反应为_____(填“吸热”或“放热”)反应。
(2)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有______(填字母序号)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com