
由黄铜矿为原料(主要成分为CuFeS2)制备99.95%~99.98%精铜的流程如下:
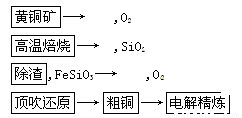
(1) 高温焙烧第一反应为2CuFeS2+4O2===Cu2S+2FeO+3SO2,该反应中氧化剂为____________。产物Cu2S在1 200℃高温下继续反应:2Cu2S+3O2===2Cu2O+2SO2,2Cu2O+Cu2S===6Cu+SO2。6mol CuFeS2和14.25mol O2反应,理论上可得到Cu________mol(假定各步反应都完全)。
(2) 取三份质量均为16.9g的上述粗铜,成分为Cu、Fe、Zn。现在需要分析其中铜的含量,进行如下实验(所有气体体积均为标况下的数据):
① 取一份粗铜放入足量稀硫酸中,共放出氢气1.568L。
② 另取一份粗铜放入稍过量的较浓硝酸中,加热使合金铜完全溶解,收集到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。
③ 再取一份粗铜进行电解精炼,阳极完全溶解后阴极增加质量17.28g。
求粗铜中Cu的质量分数(保留一位小数)。
科目:高中化学 来源:江苏省南京市金陵中学2011届高三第四次模拟考试化学试题 题型:022
由黄铜矿为原料(主要成分为CuFeS2)制备99.95%~99.98%精铜的流程如下:
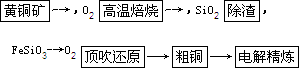
(1)高温焙烧第一反应为2CuFeS2+4O2![]() Cu2S+2FeO+3SO2,该反应中氧化剂为_________.产物Cu2S在1 200℃高温下继续反应:2Cu2S+3O2
Cu2S+2FeO+3SO2,该反应中氧化剂为_________.产物Cu2S在1 200℃高温下继续反应:2Cu2S+3O2![]() 2Cu2O+2SO2,2Cu2O+Cu2S
2Cu2O+2SO2,2Cu2O+Cu2S![]() 6Cu+SO2.6 mol CuFeS2和14.25 mol O2反应,理论上可得到Cu_________mol(假定各步反应都完全).
6Cu+SO2.6 mol CuFeS2和14.25 mol O2反应,理论上可得到Cu_________mol(假定各步反应都完全).
(2)取三份质量均为16.9 g的上述粗铜,成分为Cu、Fe、Zn.现在需要分析其中铜的含量,进行如下实验(所有气体体积均为标况下的数据):
①取一份粗铜放入足量稀硫酸中,共放出氢气1.568 L.
②另取一份粗铜放入稍过量的较浓硝酸中,加热使合金铜完全溶解,收集到了NO和NO2的混合气体8.736 L,与3.304 L O2混合后,得到的混合气体恰好被水完全吸收.
③再取一份粗铜进行电解精炼,阳极完全溶解后阴极增加质量17.28 g.
求粗铜中Cu的质量分数(保留一位小数).
查看答案和解析>>
科目:高中化学 来源: 题型:
由黄铜矿为原料(主要成分为CuFeS2)制备99.95%~99.98%精铜的流程如下:
(1) 高温焙烧第一反应为2CuFeS2+4O2===Cu2S+2FeO+3SO2,该反应中氧化剂为____________。产物Cu2S在1 200℃高温下继续反应:2Cu2S+3O2===2Cu2O+2SO2,2Cu2O+Cu2S===6Cu+SO2。6mol CuFeS2和14.25mol O2反应,理论上可得到Cu________mol(假定各步反应都完全)。
(2) 取三份质量均为16.9g的上述粗铜,成分为Cu、Fe、Zn。现在需要分析其中铜的含量,进行如下实验(所有气体体积均为标况下的数据):
① 取一份粗铜放入足量稀硫酸中,共放出氢气1.568L。
② 另取一份粗铜放入稍过量的较浓硝酸中,加热使合金铜完全溶解,收集到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。
③ 再取一份粗铜进行电解精炼,阳极完全溶解后阴极增加质量17.28g。
求粗铜中Cu的质量分数(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源:2011届江苏省南京市金陵中学高三第四次模拟考试(理综)化学部分 题型:实验题
由黄铜矿为原料(主要成分为CuFeS2)制备99.95%~99.98%精铜的流程如下: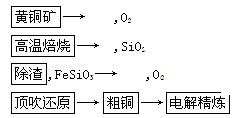
(1) 高温焙烧第一反应为2CuFeS2+4O2===Cu2S+2FeO+3SO2,该反应中氧化剂为____________。产物Cu2S在1 200℃高温下继续反应:2Cu2S+3O2===2Cu2O+2SO2,2Cu2O+Cu2S===6Cu+SO2。6mol CuFeS2和14.25mol O2反应,理论上可得到Cu________mol(假定各步反应都完全)。
(2) 取三份质量均为16.9g的上述粗铜,成分为Cu、Fe、Zn。现在需要分析其中铜的含量,进行如下实验(所有气体体积均为标况下的数据):
① 取一份粗铜放入足量稀硫酸中,共放出氢气1.568L。
② 另取一份粗铜放入稍过量的较浓硝酸中,加热使合金铜完全溶解,收集 到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。
到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。
③ 再取一份粗铜进行电解精炼,阳极完全溶解后阴极增加质量17.28g。
求粗铜中Cu的质量分数(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 -→,O2
-→,O2  -→,SiO2
-→,SiO2  ,FeSiO3-→O2
,FeSiO3-→O2 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com