
| A、7 | B、8 | C、9 | D、10 |
| 8.55 |
| 171 |
| 10.6g |
| 106g/mol |
| 8.55 |
| 171 |
| 10.6g |
| 106g/mol |
| 0.7 |
| 0.1 |


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用金属钠或者金属钾 |
| B、利用质谱法 |
| C、利用燃烧法 |
| D、利用红外光谱法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ |
| C、①②③ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A、易溶于水,也易溶于有机溶剂 |
| B、它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色 |
| C、在一定条件下它能通过加聚反应生成高分子化合物 |
| D、一定条件下1mol该物质最多可与3mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2S溶液的水解:S2-+2H2O?H2S+2OH- |
| B、碳酸溶液的电离:H2CO3?CO32-+2H+ |
| C、NH4Cl溶液的水解:NH4++H2O?NH3?H2O+H+ |
| D、NaHSO4溶液的电离:NaHSO4═Na++HSO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe的价层电子排布式为3d64s2 |
| B、35Br的电子排布式可简写为[Ar]4s24p5 |
C、NH4Cl的电子式为 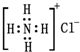 |
D、氯离子结构示意图为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸钠晶体 |
| B、不用稀硫酸,改用98%浓硫酸 |
| C、不用铁片,改用铁粉 |
| D、加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com