
【题目】下列物质中,属于能够导电的电解质是
A.铜丝B.蔗糖C.NaCl溶液D.熔融的MgCl2
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】控制“酸雨”是防治大气污染的重要问题之一。煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用Ca(ClO)2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)Ca(ClO)2中氯元素的化合价为___________。
(2)工业上制备Ca(ClO)2的化学方程式_________________________________________________。
(3)实验室在鼓泡反应器中通入含有SO2的烟气,反应温度为323 K,Ca(ClO)2溶液浓度为5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如下表:
离子 | SO42 | Cl |
c/(mol·L1) | 5×103 | 1×102 |
写出Ca(ClO)2溶液在脱硫过程中主要反应的离子方程式____________________________________。
(4)目前可用电化学方法处理由二氧化硫引起的酸雨。常见的一种方法是惰性电极电解氢溴酸,其阳极的电极反应为:___________________________________。阴极的电极反应为:_________________________________。总反应的化学方程式为:___________________________。
(5)将其阳极产物用水溶解配成溶液去淋洗含二氧化硫的废气。上述吸收废气发生的反应化学方程式为:________________________________________。若反应中转移电子1mol,则可吸收二氧化硫气体体积在标准状况下为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期主族元素原子半径与原子序数的关系图。下列说法正确的是

A. a的单质在高温条件下能置换出e的单质,说明非金属性a<e
B. b、d两种元素的简单离子半径相比,前者较大
C. 由b、e两种元素组成的化合物能溶解于强碱溶液,但不能与酸溶液反应
D. 由c、d分别与f组成的化合物中的化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质分类正确的是
酸 | 碱 | 盐 | 氧化物 | |
A | 硫酸 | 纯碱 | 硅酸钠 | 干冰 |
B | 氢硫酸 | 烧碱 | 纯碱 | 氧化铜 |
C | 碳酸 | 生石灰 | 小苏打 | 二氧化硫 |
D | 二氧化碳 | 苛性钠 | 食盐 | 石灰石 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
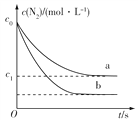
【题目】汽车尾气中NO产生的反应为N2(g)+O2(g) ![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下,N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下,N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
A. 在温度T下,该反应的平衡常数K=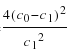
B. 在温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的反应条件改变可能是加入了催化剂
D. 若曲线b对应的反应条件改变是温度,可判断该反应的ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)把一块纯净的锌片插入盛有稀硫酸的烧杯中,可观察到锌片逐渐溶解,并有气泡产生;平行地插入一块铜片(如图甲装置所示),可观察到铜片上________(填“有”或“没有”)气泡产生;若用导线把锌片和铜片连接起来(如图乙装置所示),可观察到铜片上________(填“有”或“没有”)气泡产生。
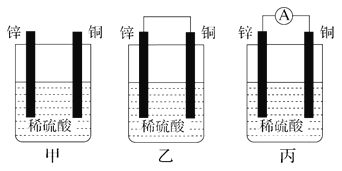
(2)用导线将电流表的两端与溶液中的锌片和铜片相连(如图丙装置所示),观察到电流表的指针发生了偏转,说明导线中有电流通过。锌片上的电极反应:______________;铜片上的电极反应:____________________________。
(3)乙、丙装置是将________能转化为________能的装置。
Ⅱ.断开1molH﹣H键,1molN﹣H键,1molN≡N键分别需要吸收的能量为436kJ、391kJ、946kJ,求:
(1)1molN2生成NH3需_____(填“吸收”或“放出”)能量_____ kJ
(2)1molH2生成NH3需_____(填“吸收”或“放出”)能量_____ kJ(不考虑可逆反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子化合物;B与Z的最外层电子数之比2:3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。请回答下列问题。
(1)Z的原子结构示意图为 ;化合物BA4的电子式为 。
(2)化合物Y2X2中含有的化学键类型有 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)化合物A2X和A2Z中,沸点较高的是 (填化学式),其主要原因是 。
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将9.6g铜单质置于200mL一定浓度的稀硝酸中,两者恰好完全反应.假定溶液体积不变,请回答下列问题:(要求写出计算过程) 
(1)反应生成的气体的体积(标况下);
(2)反应过程中转移电子的物质的量;
(3)参加反应的稀硝酸的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2 H2O(g)![]() 2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2 H2(g) + O2(g) H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
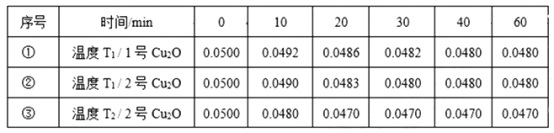
下列说法不正确的是
A. 实验时的温度T2高于T1
B. 2号Cu2O的催化效率比1号Cu2O的催化效率高
C. 实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol·Lˉ1·minˉ1
D. 等质量纳米级Cu2O比微米级Cu2O催化效率高,这与Cu2O的粒径大小有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com