
【题目】用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液。
(1)已知:黄铁矿中的硫元素在酸性条件下可被![]() 氧化成
氧化成![]() ,若生成标准状况下3.36 L ClO2气体,至少需要黄铁矿的质量为 。
,若生成标准状况下3.36 L ClO2气体,至少需要黄铁矿的质量为 。
(2)工业上以“m(ClO2)/m(NaClO3)”作为衡量ClO2产率的指标。若取NaClO3样品3.0 g,通过反应和吸收获得200 mL ClO2溶液,取此溶液20 mL与37.00 mL 0.500 mol·L-1 (NH4)2Fe(SO4)2溶液充分反应后,过量的Fe2+再用0.040 0 mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7标准溶液25.00 mL。
①写出ClO2溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式 。
②试计算ClO2的“产率”(写出计算过程) 。
【答案】
(1)1.2 g(3分)
(2)①4H++ClO2+5Fe2+===Cl-+5Fe3++2H2O(3分)
②由 Cr2O![]() ~ 6Fe2+
~ 6Fe2+
n(Fe2+)= 6n(Cr2O![]() )=6×0.04 mol·L-1×25 mL×10-3=6×10-3 mol
)=6×0.04 mol·L-1×25 mL×10-3=6×10-3 mol
由ClO2 ~ 5Fe2+
n(ClO2)= 1/5n(Fe2+) =(0.5 mol·L-1×37 mL×10-3-6×10-3 mol)÷5=2.5×10-3 mol
所以,ClO2的产率=[(2.5×10-3 mol×10×67.5 g·mol-1)/3.0 g]×100%=56.25%(6分)
【解析】
试题分析:
(1)根据反应15![]() +FeS2+14H+===15ClO2+Fe3++7H2O+2
+FeS2+14H+===15ClO2+Fe3++7H2O+2![]() ,知n(FeS2)=
,知n(FeS2)= ![]() n(ClO2)=3.36/22.4/15=0.01 mol,m(FeS2)=0.01 mol×120 g/mol=1.2 g。
n(ClO2)=3.36/22.4/15=0.01 mol,m(FeS2)=0.01 mol×120 g/mol=1.2 g。
(2)①ClO2为氧化剂,产物为Cl-,Fe2+应转化为Fe3+,故方程式为4H++ClO2+5Fe2+=Cl-+5Fe3++2H2O
②该反应的原理是利用过量亚铁离子把ClO2还原,根据n(Fe2+)的量计算ClO2,根据公式计算产率。
剩余Fe2+的量
由 Cr2O![]() ~ 6Fe2+
~ 6Fe2+
n(Fe2+)= 6n(![]() )=6×0.04 mol·L-1×25 mL×10-3=6×10-3 mol
)=6×0.04 mol·L-1×25 mL×10-3=6×10-3 mol
与ClO2反应的Fe2+的量
n(Fe2+) =0.5 mol·L-1×37 mL×10-3-6×10-3 mol
由ClO2 ~ 5Fe2+
n(ClO2)= 1/5n(Fe2+) =(0.5 mol·L-1×37 mL×10-3-6×10-3 mol)÷5=2.5×10-3 mol
所以,ClO2的产率=[(2.5×10-3 mol×10×67.5 g·mol-1)/3.0 g]×100%=56.25%。


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
【题目】某硫酸镁和硫酸铝的混合溶液中,c(Mg2+ )=2 mol·L-1,c(SO42-)=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+分离,至少应加入1.6 mol·L-1氢氧化钠溶液的体积是
A.0.5 L B.1.625 LC.1.8 LD.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原电池和电解池的叙述中,正确的是
A.纯锌与稀硫酸的反应比Zn-Cu合金与稀硫酸的反应更快
B.钢铁发生吸氧腐蚀时,负极的反应式为:Fe-3e-=Fe3+
C.在铁制容器上镀铜时,铁制容器连接外接电源的正极
D.电解精炼铜时,阴极的电极反应为:Cu2+ + 2e-=Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解已广泛应用于金属冶炼、污水的处理等工业。
(1)新型的钛基纳米PbO2电极材料制备:在钛板上先形成一层铝膜,在草酸溶液中作阳极氧化为氧化铝同时形成孔洞,再在Pb(NO3)2溶液中浸泡电解形成纳米PbO2,用氢氧化钠溶液浸泡除去多余的氧化铝,获得钛基纳米PbO2电极。
①钛基板打磨后用丙酮浸泡,再用水冲洗,用丙酮浸泡的作用是 。
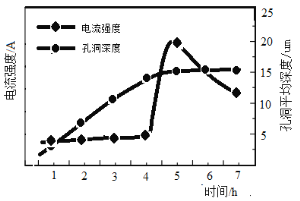
②阳极氧化时溶液中电流强度和基板孔洞深度随时间变化如下图所示,氧化的终点电流突然增加的原因是 。电极氧化成孔洞时温度需严格控制在8℃左右,温度不宜过高的原因是 。
③电解形成纳米PbO2时阳极电极反应式为 。工业上可以用Na2S2O8溶液氧化Pb(NO3)2制备PbO2,其离子方程式为 。
(2)PbO2做阳极电解处理污水
①用PbO2材料做阳极处理污水的效果明显优于石墨电极,其原因可能是 。
②某小组用自己制作的钛基纳米PbO2电极电解处理污水,发现污水澄清效果优于购买的标准钛基纳米PbO2电极。此钛基纳米PbO2电极的EDX能图谱信息如下图,其去污效果好的原因可能是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。
(1)常温下,可用铁或者铝制的容器盛放浓硝酸,说明浓硝酸具有_________ 性
A.酸性 B.强氧化性 C.吸水性 D.脱水性
(2)工业上用洗净的废铜屑作原料来制备硫酸铜。下列制备方法符合“绿色化学”思想的是_______________________________(填序号)。
① Cu + H2SO4(浓)![]() CuSO4 ② Cu
CuSO4 ② Cu![]() CuO
CuO![]() uSO4
uSO4
写出①中反应的化学方程式:________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4P(红磷s)![]() P4(白磷s) △H = +17kJmol﹣1根据以上方程式,下列推论正确的是
P4(白磷s) △H = +17kJmol﹣1根据以上方程式,下列推论正确的是
A. 正反应是一个放热反应
B. 当lmol白磷完全转变成红磷时放出17kJ热量
C. 当4g红磷转变成白磷时吸收17kJ热量
D. 白磷比红磷稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物在工农业上有重要作用。
(1)水煤气是将水蒸气通过灼热的焦炭而生成的气体,水煤气的主要成分为_________
(用化学式表示);
(2)高温时,用CO还原MgSO4可制备高纯度MgO。若在750℃时,测得气体中含有等物质的量的SO2、SO3,则反应的化学方程式为____________;
(3)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由CO2制取碳的太阳能工艺如右图所示。

①若“重整系统”发生的反应中![]() =6,则FexOy的化学式为____________;
=6,则FexOy的化学式为____________;
②“热分解系统”中每分解1mol FexOy,转移电子的物质的量为____________。
(4)工业上用CO2和H2反应合成甲醚。
已知:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) ΔH=130.8 kJ·mol-1
CH3OCH3(g)+3H2O(g) ΔH=130.8 kJ·mol-1
①一定条件下,上述合成甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是____________(填标号)。
a.逆反应速率先增大后减小 b.反应物的体积百分含量减小
c.H2的转化率增大 d.容器中的n(CO2)/n(H2)值变小
②某压强下,合成甲醚的反应在不同温度、不同投料比时,CO2的转化率如图所示。

T1温度下,将4molCO2和8molH2充入2L的密闭容器中,5min后该反应达到平衡,则0~5min内的平均反应速率v(CH3OCH3)=______________;
KA、KB、KC三者之间的大小关系为_____________。
(5)常温下,用氨水吸收CO2可得到NH4HCO3溶液,在该溶液中,c(NH4+)________(填“>”、“<”或“=”)c(HCO3-;反应NH4++HCO3+H2O![]() NH3·H2O+H2CO3的平衡常数K=__________。
NH3·H2O+H2CO3的平衡常数K=__________。
(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7,K2=4×10-11)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com