
有关键能数据如表所示:
| 化学键 | N≡N | H—H | H—N |
| 键能/kJ·mol-1 | x | 436 | 391 |
 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:单选题
下列依据热化学方程式得出的结论正确的是( )
| A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ· mol—1则氢气的燃烧热为△H=-241.8 kJ· mol—1 |
| B.已知C(石墨,s)=C(金刚石,s);△H=+1.9kJ·mol-1,可知石墨比金刚石更稳定 |
| C.已知NaOH(ag)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4 kJ· mol—1可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.4 kJ |
| D.已知2C(s)+2O2(g)=2CO2(g);△H1 2C(s)+O2(g)=2CO(g);△H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
分析右图的能量变化示意图,下列选项正确的是
| A.2A+B═2C;△H>O |
| B.2C═2A+B;△H<0 |
| C.2A(g)+B(g)═2C(g)△H>0 |
| D.2A(g)+B(g)═2C(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法或表示方法正确的是
| A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由“C(石墨)=C(金刚石) ΔH=1.9kJ/mol”可知,金刚石比石墨稳定 |
| C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,若将含1molCH3COOH与含1mol NaOH的溶液混合,放出的热量小于57.3kJ |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=—285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
红磷(P)和Cl2发生反应生成PCl3和PCl5,反应过程和能量的关系如下图所示,图中的ΔH表示生成1 mol产物的数据。已知PCl5分解生成PCl3和Cl2,该分解反应是可逆反应。下列说法正确的是 ( )
| A.其他条件不变,升高温度有利于PCl5的生成 |
| B.反应2P(s)+5Cl2(g)=2PCl5(g)对应的反应热 ΔH=-798 kJ·mol-1 |
| C.P和Cl2反应生成PCl3的热化学方程式为2P(s)+3Cl2(g)=2PCl3(g) ΔH=-306 kJ·mol-1 |
| D.其他条件不变,对于PCl5分解生成PCl3和Cl2的反应,增大压强,PCl5的转化率减小,平衡常数K不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知1g氢气完全燃烧生成水蒸气时放出121kJ的能量,且氧气中1molO=O键完全断裂时需要吸收496kJ的能量,水蒸气中1mol H—O键形成时放出463kJ的能量,则氢气中1mol H—H键断裂时吸收的能量为( )
| A.920kJ | B.557kJ | C.436kJ | D.181kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见 ( )
| A.NH4HCO3和盐酸的反应是放热反应 |
| B.该反应中,热能转化为产物内部的能量 |
| C.反应物的总能量高于生成物的总能量 |
| D.反应的热化学方程式为NH4HCO3+HCl―→NH4Cl+CO2↑+H2O ΔH=+Q kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
红磷(P)和Cl2发生反应生成PCl3和PCl5,反应过程和能量的关系如下图所示,图中的ΔH表示生成1 mol产物的数据。已知PCl5分解生成PCl3和Cl2,该分解反应是可逆反应。下列说法正确的是( )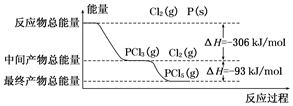
| A.其他条件不变,升高温度有利于PCl5的生成 |
| B.反应2P(s)+5Cl2(g)=2PCl5(g)对应的反应热 ΔH=-798 kJ/mol |
| C.P和Cl2反应生成PCl3的热化学方程式为:2P(s)+3Cl2(g)=2PCl3(g) ΔH=-306 kJ/mol |
| D.其他条件不变,对于2PCl5(g)=2P(s)+5Cl2(g) ΔH反应,增大压强,PCl5的转化率减小,ΔH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示,下列说法不正确的是( )
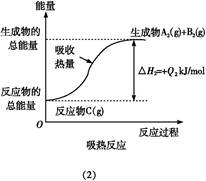
A.反应过程(1)的热化学方程式为A2(g)+B2(g) C(g)ΔH1=-Q1 kJ/mol C(g)ΔH1=-Q1 kJ/mol |
B.反应过程(2)的热化学方程式为C(g) A2(g)+B2(g)ΔH2=+Q2 kJ/mol A2(g)+B2(g)ΔH2=+Q2 kJ/mol |
| C.Q1与Q2的关系:Q1>Q2 |
| D.ΔH2>ΔH1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com