
【题目】下列有关常见的几种金属氧化物的性质和用途的说法不正确的是( )
A. 氧化钙可用作干燥剂 B. Fe2O3可用于制作红色油漆和涂料
C. MgO和Al2O3可用作耐高温材料 D. Na2O2、CuO、FeO都能溶于水,且与水反应都生成相应的碱
科目:高中化学 来源: 题型:
【题目】甲酸、乙酸、碳酸、苯酚的酸性由强到弱的顺序是( )
A.碳酸、苯酚、甲酸、乙酸B.甲酸、乙酸、碳酸、苯酚
C.甲酸、碳酸、苯酚、乙酸D.苯酚、碳酸、乙酸、甲酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化不可能通过一步实验直接完成的是
A. Al(OH)3→Al2O3 B. Al2O3→Al(OH)3 C. Al→Al2O3 D. AlCl3→Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( ) 
A.该硫酸的物质的量浓度为9.2 mol/L
B.1 mol Zn与足量该硫酸反应产生2 g氢气
C.配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL
D.该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,ag气体A与bg气体B的分子数相等,則下列说法中不正确的是( )
A.A和B的相对分子质最之比为a:b
B.同温同压下,A和B的原子数之比为b:a
C.同质量的A和B的物质的量之比为b:a
D.同温同压下,同体积的A和B的质量之比为a:b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g) ![]() 2Z(g) ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是( )
2Z(g) ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是( )
A. 升高温度,X的体积分数减小
B. 增大压强(缩小容器体积),Z的浓度不变
C. 保持容器体积不变,充入一定量的惰性气体,Y的浓度不变
D. 保持容器体积不变,充入一定量的Z,X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
![]()
该反应在研究新型发光材料、超分子化学等方面具有重要价值。如图是用利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的化学名称为______________________________。
(2)③的反应类型为_________________________________。
(3)E的结构简式为__________________________________________________。用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气________________________________mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中2种的结构简式_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式或说法正确的是( )
A. 甲烷的燃烧热为ΔH=-890 kJ·mol-1 ,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890 kJ· mol-1
B. 500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C. 已知:H2(g)+F2(g)=2HF(g) ΔH=-270 kJ·mol-1 ,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ
D. 在C中相同条件下,2 mol HF气体的能量小于1 mol氢气与1 mol氟气的能量总和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置. 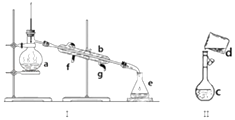
(1)写出下列仪器的名称:a.b.c. .
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 , 将仪器补充完整后进行实验,温度计水银球的位置在处.冷凝水由(填f或g)口通入.
(3)现需配制0.1mol/L CuSO4溶液450mL,装置II是某同学转移溶液的示意图.
①图中的错误是 . 除图中给出的仪器和分析天平外,为完成实验还需的仪器有: .
②根据计算得知,需称取的胆矾的质量为g.
③在100mL某浓度的CuSO4溶液中加入一质量为45.0g的铁棒,反应一段时间后,取出洗净,干燥后称量,称得质量变为46.6g.若反应后溶液的体积不变,所得溶液中FeSO4的物质的量浓度为mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com