
【题目】为了改善环境,科学家投入了大量的精力研究碳、氮及其化合物的转化。请回答下列有关问题:
(1)利用N2与H2合成氨是重要的工业反应,下图为反应过程中的能量变化关系。
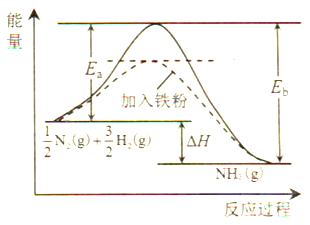
①反应中加入铁粉可以提高反应速率,其原因是____________。
②已知某些化学键键能数据如下表:
化学键 | H-H | N≡N | N-H |
E/(kJ/mol) | 436 | 946 | 391 |
反应![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g)的活化能Ea=254kJ/mol,则反应NH3(g)
NH3(g)的活化能Ea=254kJ/mol,则反应NH3(g)![]()
![]() N2(g)+
N2(g)+![]() H2(g)的活化能Eb=______kJ/mol。
H2(g)的活化能Eb=______kJ/mol。
(2)汽车内燃机工作时会将N2转化为NO,反应式为N2(g)+O2(g) ![]() 2NO(g),该反应在不同温度下的平衡常数K如下表:
2NO(g),该反应在不同温度下的平衡常数K如下表:
温度 | 27℃ | 2000℃ |
K | 3.8×10-31 | 0.1 |
温度为2000℃,某时刻测得反应体系中各物质的浓度分别为c(N2)=0.2mol/L,c(O2)=0.03mol/L,c(NO)=0.03mol/L,此时该反应的速率(v)应满足的关系为_______(填字母序号)。
A.v正>v逆 B.v正=v逆 C.v正<v逆 D.无法确定
(3)工业上可将CO转化成甲醇,反应式为:CO(g)+2H2(g)![]() CH3OH(g)。若在一容积可变的密闭容器中充入1molCO和2molH2进行反应,初始体积为3L,保持压强不变,反应后CO的平衡转化率随温度(T)的变化如右图中曲线所示。
CH3OH(g)。若在一容积可变的密闭容器中充入1molCO和2molH2进行反应,初始体积为3L,保持压强不变,反应后CO的平衡转化率随温度(T)的变化如右图中曲线所示。

①若所加的CO和H2的量以及反应温度均不变,则达到平衡状态A、B时的压强pA____pB(填“>”、“<”或“=”),其原因是___________________。
②若达到化学平衡状态A时,CO的体积分数为25%,此时CO的转化率为_____;平衡常数KA=________。
【答案】 降低了合成氨反应的活化能 300 C < 该反应为气体分子数减小的反应,增大压强,有利于平衡向正向移动。CO转化率升高,故pA<pB 50% 4L2/mol2
【解析】(1)①通过图像可出铁粉作催化剂,降低了合成氨反应的活化能,提高了反应速率;正确答案:降低了合成氨反应的活化能。
②针对反应![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g) ![]() NH3(g),反应热=反应物断键吸收的总能量-生成物成键放出的总能量=436×1.5+946×0.5-3×391=-46 kJ·mol-1;反应热=Ea-Eb=-46,254-Eb=-46,Eb=300 kJ·mol-1,所以反应NH3(g)
NH3(g),反应热=反应物断键吸收的总能量-生成物成键放出的总能量=436×1.5+946×0.5-3×391=-46 kJ·mol-1;反应热=Ea-Eb=-46,254-Eb=-46,Eb=300 kJ·mol-1,所以反应NH3(g) ![]()
![]() N2(g) +
N2(g) + ![]() H2(g) 的活化能Eb=300 kJ·mol-1;正确答案:300。
H2(g) 的活化能Eb=300 kJ·mol-1;正确答案:300。
(2) 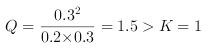 ,平衡逆向移动,v(正)
,平衡逆向移动,v(正)![]() (逆),正确答案:C。
(逆),正确答案:C。
(3) ①该反应为气体分子数减小的反应,增大压强,平衡右移,CO转化率升高,所以根据图像可知:PA小于pB;正确答案:< ;该反应为气体分子数减小的反应,增大压强,有利于平衡向正向移动。
② 设一氧化碳的变化量为X mol;
CO(g)+2H2(g) ![]() CH3OH(g)。
CH3OH(g)。
起始量 1 2 0
变化量 X 2X X
平衡量 1-X 2-2X X
若达到化学平衡状态A时,CO的体积分数为25%,(1-X)/(1-X+2-2X+X)= 0.25,X=0.5mol, 此时CO的转化率为0.5/1×100%=50%;根据气体的总量和体积成正比规律:反应前混合气体为3mol,体积为3L,反应后混合气体为2 mol,体积为2L,平衡后各物质浓度为c(CH3OH)=0.5/2=0.25mol/L, c(CO)=0.5/2=0.2mol/L, c(H2)=1/2=0.5mol/L,平衡常数KA=c(CH3OH)/c(CO)c2(H2)=0.25/0.25×(0.5)2= 4L2/mol2;正确答案:50%; 4L2/mol2。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设nA代表阿伏伽德罗常数(NA)的数值,下列说法正确的是( )
A.22.4L中含有nA个分子
B.1L0.1mol/LNa2SO4溶液中有0.1个Na+
C.1molH2与1molCl2反应生成nA个HCl分子
D.1molCa变成Ca2+时失去的电子数为2nA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列各题
(1)铵态氮肥不稳定,受热易分解.写出氯化铵(NH4Cl)受热发生分解反应的化学方程式 .
(2)乙烯能使溴水褪色,生成1,2﹣二溴乙烷(CH2 Br﹣CH2 Br).写出该反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)在l0L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率
4NO(g)+6H2O(g)在l0L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率![]() 可表示为
可表示为
A. ![]() =0.010mol/(L·s) B.
=0.010mol/(L·s) B. ![]() =0.0010 mol/(L·s)
=0.0010 mol/(L·s)
C. ![]() =0.0010 mol/(L·s) D.
=0.0010 mol/(L·s) D. ![]() =0.0045 mol/(L·s)
=0.0045 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在标准状况下,气体摩尔体积约为22.4L/mol。则在常温常压下(25℃,101kPa)0.2mol气体A的体积为 ( )
A.4.48LB.大于4.48LC.小于4.48LD.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五水硫酸铜(CuSO4·5H2O)和六水硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]都是重要的化工原料,用途十分广泛。
请回答与这两种物质中元素有关的一些问题。
(1)基态铁原子的核外电子排布式为_______;基态铜原子的电子占据的最高能层符号为_______ 。
(2)氧元素的第一电离能小于氮元素,其原因是_______ 。
(3)SO42-、H2O、NH4+三种微粒中,空间构型为正四面体的是_______;NH4+中氮原子的杂化轨道类型是_______。
(4)写出与SO42-互为等电子体的分子的化学式_______ (写一种)。
(5)Cu与Au的合金可形成面心立方最密堆积的晶体,在该晶胞中Cu原子处于面心,该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为_______,若该晶体的密度为ρg.cm-3,则晶胞中Cu原子与Au原子中心的最短距离d=_______cm(NA表示阿伏加德罗常数的值)。
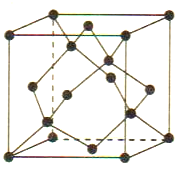
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为:K= ![]() ,有关该平衡体系的说法正确的是( )
,有关该平衡体系的说法正确的是( )
A.该反应可表示为X(g)+2Y(g)═2Z(g)+2W(g)
B.减小X浓度,平衡向逆反应方向移动,平衡常数K减小
C.增大反应容器的压强,该反应速率一定增大
D.升高温度,W(g)体积分数增加,则正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关甲烷的叙述正确的是( )
A.甲烷不能使高锰酸钾酸性溶液褪色,所以甲烷不能发生氧化反应
B.甲烷与氯气的取代反应,生成的产物中CH3Cl最多
C.CH4的键角均为10928,可以说明甲烷分子是以碳原子为中心的正四面体结构,而不是平面正方形结构
D.甲烷、乙烷、丙烷是同系物,它们中的化学键都是极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取少量某镁铝合金粉末,其组成可用MgxAly表示,向其中加入足量稀硫酸充分反应,收集到3.808L H2(标准状况)同时得无色溶液,向所得溶液中加入过量NaOH溶液,充分反应得到沉淀4.64g。则x∶y为
A. 2∶1 B. 4∶3 C. 1∶1 D. 1∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com