
【题目】在标准状况下①6.72L CH4②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3 , 下列对这四种气体的关系从大到小表达正确的是( )
A.体积②>③>①>④
B.密度②>③>①>④
C.质量②>①>③>④
D.氢原子个数①>③>②>④
【答案】A
【解析】解:①6.72L CH4 物质的量为 ![]() =0.3mol,②3.01×1023个HCl分子的物质的量为0.5mol,③13.6g H2S 的物质的量为
=0.3mol,②3.01×1023个HCl分子的物质的量为0.5mol,③13.6g H2S 的物质的量为 ![]() =0.4mol,④0.2mol NH3 . A.相同条件下,气体的体积之比等于物质的量之比,所以体积体积②>③>①>④,故A正确;
=0.4mol,④0.2mol NH3 . A.相同条件下,气体的体积之比等于物质的量之比,所以体积体积②>③>①>④,故A正确;
B.各物质的摩尔质量分别为①CH4 为16g/mol②HCl为36.5g/mol ③H2S 为34g/mol④NH3为17g/mol,相同条件下,密度之比等于摩尔质量之比,所以密度②>③>④>①,故B错误;
C.各物质的质量分别为①CH4 为0.3mol×16g/mol=4.8g,②HCl为0.5mol×36.5g/mol=18.25g,③H2S 13.6g,④NH3为0.2mol×17g/mol=3.4g,所以质量②>③>①>④,故C错误;
D.各物质中H原子的物质的量分别为①CH4 为0.3mol×4=1.2mol②HCl为0.5mol③H2S 0.4mol×2=0.8mol④NH3为0.2mol×3=0.6mol,所以氢原子个数①>③>④>②,故D错误.
故选A.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某烃室温时为气态,完全燃烧后,生成的H2O和CO2的物质的量之比为3∶4。该不饱和烃的链状同分异构体的数目是( )
A.2种B.3种C.4种D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属及其化合物的说法正确的是
A. 钠保存在煤油里的原因之一是它极易与氧气反应
B. 食品工业中用Na2CO3作焙制糕点的膨松剂
C. 镁表面的氧化膜疏松,不能保护内层金属
D. 铝在空气中很容易燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应.硼与氯气反应生成三氯化硼(BCl3),生成的三氯化硼遇水水解产生白雾(BCl3+3H2O=H3BO3+3HCl)(已知:BCl3的熔点为﹣107.3℃,沸点为12.5℃),且三氯化硼用于制取乙硼烷(B2H6).某兴趣小组设计如图所示装置制备三氯化硼. 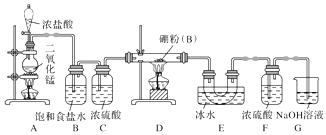
回答下列问题:
(1)盛浓盐酸的装置名称为 .
(2)装置E的作用是
(3)装置D中发生反应的化学方程式为 .
(4)装置F的作用是 , 可以用一个盛装(填试剂名称)的干燥管代替装置F和G,使实验更简便.
(5)为了顺利完成实验,点燃酒精灯的正确操作是(填字母),其理由是 . a.先点燃A处酒精灯,后点燃D处酒精灯
b.先点燃D处酒精灯,后点燃A处酒精灯
c.同时点燃A、D两处酒精灯.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒和钛金属的性能都很优越,在航空航天领域用途广泛。回答下列问题:
(1)钛元素基态原子的电子排布式为______________,未成对电子数为_______________个。
(2)[TiO(H2O2)2]2+配离子呈黄色。提供中心原子孤电子对的成键原子是_____________(填元素符号),中心原子的化合价为_____________;配体之一H2O2中氧原子杂化类型为__________,H2O2分子中氧原子的价层电子对互斥模型是______________。
(3)单质钒及钛都是由______________键形成的晶体,己知金属钛是六方最密堆积,金属钒是体心立方堆积,则__________(填“钛”,或“钒”)的空间利用率较大。
(4)碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图所示。
 (小球为V原子)
(小球为V原子)
①晶胞中碳原子与钒原子的数量比为____________。
②该晶胞中与碳原子距离最近且相等的碳原子个数为_____________。
③若合金的密度为dg· cm-3,晶胞参数α=______nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来“雾霾”污染日益严重,原因之一是机动车尾气中含有NO、NO2、CO等气体,火力发电厂释放出大量的NOx、SO2和CO2等气体也是其原因,现在对其中的一些气体进行了一定的研究:
(1)用 CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:①CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) △H = - 574 kJ/mol
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) △H = - 1160 kJ/mol
③H2O(g) = H2O(l) △H = - 44.0 kJ/mol
写出 CH4(g)与 NO2(g)反应生成 N2(g)、CO2(g)和 H2O(l)的热化学方程式: _____________________________________________________________。
(2)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体。4CO(g)+2NO2(g) ![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是________________(填代号)。

(3)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH=a kJ/mol
N2(g)+CO2(g) ΔH=a kJ/mol
在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率v(NO)=_____________________;计算该反应的平衡常数K=____________________。
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是_________(填字母代号)。
A.通入一定量的CO2 B.加入合适的催化剂
C.适当缩小容器的体积 D.通入一定量的NO
E.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:1:1,则达到新平衡时NO的转化率____________(填“升高”或“降低”),a________0(填“>”或“<”)。
(4)温度T1和T2时,分别将0.50 mol CH4和1.2mol NO2充入1 L的密闭容器中发生反应:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H=bkJ/mol。
N2(g)+CO2(g)+2H2O(g) △H=bkJ/mol。
测得有关数据如下表:
温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
下列说法正确的是__________________。
A.T1>T2,且b>0
B.当温度为T2、反应进行到40 min时, x>0.15
C.温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)<0.70mol
D.温度为T1时,若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50molH2O(g),反应开始时,ν(正)>ν(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将A2和B2两种气体通入1 L密闭容器中发生反应:xA2(g)+yB2(g)=2C(g),2 s时测得v(A2)=0.4 mol·L-1 s-1,v(B2)=1.2 mol L-1 s-1,v(C)=0.8 mol L-1 s-1。则x和y的值分别为
A. 1和3 B. 3和2 C. 3和1 D. 2和3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com