
某研究性学习小组的同学通过课外学习了解到:某品牌牙膏中含有摩擦剂、湿润剂、表面活性剂、黏合剂、香料、甜味剂等成分,其中的摩擦剂除了含CaCO3外,可能还含有Al(OH)3、SiO2中的一种或两种。为探究该品牌牙膏中摩擦剂的成分,该小组的同学进行了如下实验(牙膏中其他成分遇到盐酸时无气体产生):

请回答下列问题:
(1)操作Ⅰ中涉及的玻璃仪器有烧杯、________、________
(2)写出下列操作Ⅳ的离子方程式:______________________________
(3)该摩擦剂中除CaCO3外,肯定含有__________________
(4)为进一步探究摩擦剂中碳酸钙的含量,该小组同学利用如图所示装置(图中夹持仪器略去)进行实验。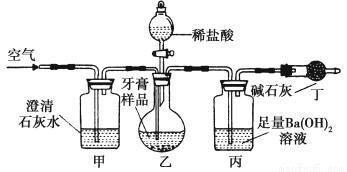
请回答下列问题:
①实验过程中需持续缓缓通入空气。其作用除了可充分混合装置乙和丙中的反应物外,还有________的作用;
②丙中主要反应的化学方程式是_______________
③实验中准确称取4.00 g样品三份,进行三次测定,测得BaCO3的平均质量为1.97 g,计算样品中碳酸钙的质量分数:__________________________
④有同学认为只要测定装置丙在吸收CO2前后的质量差,不必测定装置丙中生成的BaCO3质量,一样可以确定碳酸钙的质量分数。你认为该方案是否可行?________,简述理由:________。
科目:高中化学 来源:2016届山东省高三12月月考化学试卷(解析版) 题型:选择题
单质或化合物A可能为Na、C 、Si、 N2 、H2S,可以实现下列转化关系的有( )
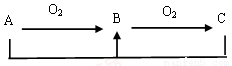
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州十校联合体高一上学期期中测试化学试卷(解析版) 题型:选择题
已知aAm+与bBn-具有相同的核外电子排布,则下列关系正确的是
A. a=b+m+n B. a=b-m+n C. a=b+m-n D. a=b-m-n
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期10月阶段测化学试卷(解析版) 题型:实验题
二氧化氯(ClO2黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问题:
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为 。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制各ClO2:


己知:NCl3中Cl元素化合价为+1价,具有强氧化性
①电解时发生反应的化学方程式为 。
②溶液X中大量存在的阴离子有 。
③除去ClO2中的NH3可选用的试剂是 (填标号)。
A、水 B、碱石灰 C、浓硫酸 D、饱和食盐水
(3)用下图装置可以测定混合气中ClO2的含量:
I、在锥形瓶中加入足量的碘化钾,用50mL水溶解后,再加入3mL稀硫酸;
II、在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
III、.将一定量的混合气体通入锥形瓶中吸收;
IV、将玻璃液封装置中的水倒入锥形瓶中;
V、用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I- +S4O62-),指示剂显示终点时共用去20.00mL硫代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为 。
②玻璃液封装置的作用是 。
③V中加入的指示剂通常为 ,滴定至终点的现象是 。
④测得混合气体中ClO2的质量为 g。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川市高三上学期统练(三)化学试卷(解析版) 题型:选择题
用NaOH溶液滴定盐酸时,由于滴定速度太快,当混合溶液变红时不知NaOH是否过量,判断它是否过量的方法是
A.加入5mL盐酸再进行滴定 B.返滴一滴待测盐酸
C.重新进行滴定 D.以上方法均不适用
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师范大学附属中学高三上学期期中考试化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A. 标准状况下2.24L氯气与水充分反应转移电子数为0.1NA
B. 标况下,2.24LNO2分子总数小于0.1NA
C. 标准状况下2.24L的CCl4中含有的C—Cl键数为0.4NA
D. 6.8g液态KHSO4中含有0.1NA个阳离子
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第三次考试化学试卷(解析版) 题型:填空题
H、C、N、O、Fe、Si、I是中学化学中常见的元素,请根据题意回答与这些元素有关的问题:
(1)根据元素周期律,碳的非金属性强于硅,请用一个化学反应方程式表示___________________。
(2)若FeSO4和O2的系数比为2:1,试配平下列方程式:__FeSO4+__K2O2→__K2FeO4+__K2O+__K2SO4+__O2↑
(3)各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氮氧化物(NOX)废气的方法之一是用NaOH溶液进行吸收,其反应原理可表示如下:NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
现有一NO与NO2的混合气体,将其通入50mL 2mol/L的NaOH溶液中,恰好完全吸收,测得溶液中含有NO3― 0.02mol。
①所得溶液中NaNO2的物质的量为 mol;
②混合气体中V(NO):V(NO2)= 。
(4)向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)的变化可用下图简单表示
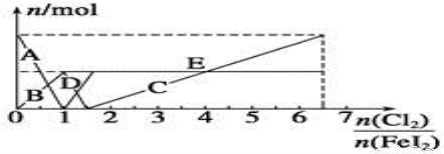
①当n(Cl2)∶n(FeI2)=6.5时,溶液中n(Cl-)∶n(IO3-)= 。
②当n(Cl2)∶n(FeI2)=1.2时,离子方程式可表示为 。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:选择题
下列有关化学用语表述正确的是
A.S2-的结构示意图:
B.Na2S的电子式:
C.邻羟基苯甲酸的结构简式:
D.质子数与中子数相等的硫原子: S
S
查看答案和解析>>
科目:高中化学 来源:2016届陕西西安第一中学高三上学期期中考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1的KNO3溶液:H+、FE2+、Cl-、SO42-
B.饱和氯水中:NH4+、SO32-、SO42-、Cl-
C.C(H+)=1.0×10-13mol/L溶液中:K+、NA+、CH3COO-、Br-
D.与铝反应产生大量氢气的溶液:NA+、K+、CO32-、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com