
(3分)工业上冶炼金属铁的主要反应为:Fe2O3 + 3CO =" 2Fe" + 3CO2。其中,Fe2O3 __________(填“被氧化”或“被还原”),CO作_________(填“氧化剂”或“还原剂”)。在该反应中,若消耗了1 mol Fe2O3,则生成__________mol Fe。
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市日坛中学高二上学期期中考试文科化学试卷(带解析) 题型:填空题
(3分)工业上冶炼金属铁的主要反应为:Fe2O3 + xCO 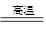 2Fe + 3CO2
2Fe + 3CO2
其中该化学方程式中x的数值是 , CO作 (填“氧化剂”或“还原剂”)。在该反应中,若消耗了1 mol Fe2O3,则生成 mol Fe。
查看答案和解析>>
科目:高中化学 来源:2015届北京市高一上学期期末考试化学试卷(解析版) 题型:填空题
(3分)工业上冶炼金属铁的主要反应为:Fe2O3 + 3CO =" 2Fe" + 3CO2。其中,Fe2O3 __________(填“被氧化”或“被还原”),CO作_________(填“氧化剂”或“还原剂”)。在该反应中,若消耗了1 mol Fe2O3,则生成__________mol Fe。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com