
 �ö������ȣ�CLO2������������ Na2FeO4Ħ������Ϊ166g•mol-1������
�ö������ȣ�CLO2������������ Na2FeO4Ħ������Ϊ166g•mol-1���������� ��1���Ե�λ���������������õ��ĵ���������ʾ����Ч�ʣ���������Ϊm������Ч�ʷֱ�Ϊ$\frac{m}{67.5}$��5��$\frac{m}{166}$��3��$\frac{m}{71}$��2��1��
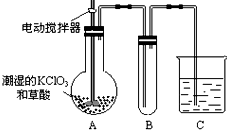
��2���������Ʊ���ԭΪ�����ӣ�������ˮ�����ɽ��壬���������ԣ�
��3���ٶ������ȵķе�ͣ�BΪClO2������װ�ã�Bװ��Ӧ�����¶ȣ�
��CΪβ������װ�ã���ѡ���������β��������������ԭ��Ӧ��
��4��Na2O2Ͷ�뵽AlCl3��Һ�У�Na2O2��ˮ����������ԭ��Ӧ�����������ƺ������������������Ȼ�����Ӧ��������������������������Ϊ����������������������Ʒ�Ӧ���ܽ⣻
�ٷ���������ԭ��Ӧ���ǹ������ƺ�ˮ�ķ�Ӧ���ݴ˼������ת�ƣ�
��0.5moLNa2O2Ͷ��lOOmL 3mol/LALCL3��Һ�У�2Na2O2+2H2O�T4NaOH+O2����������������1molNaOH��n��Al3+��=0.1L��3mol/L=0.3mol��������ȫ��������Ҫ��������0.9mol��������0.1mol�������ƻ��ܽ�0.1mol������������ƫ�����ƣ�����ֱƽ��д���ӷ���ʽ��
��� �⣺��1���Ե�λ���������������õ��ĵ���������ʾ����Ч�ʣ���������Ϊm��ClO2��Na2FeO4��Cl2��������ɱ����������Ч�ʷֱ�Ϊ$\frac{m}{67.5}$��5��$\frac{m}{166}$��3��$\frac{m}{71}$��2��1�������ɴ�С��˳��ΪClO2��Cl2��Na2FeO4���ʴ�Ϊ��ClO2��Cl2��Na2FeO4��
��2����������֮�����ܾ�ˮ��������������ǿ�������⣬��һ��ԭ������Ǹ������ƵĻ�ԭ����Fe3+��ˮ������Fe��OH��3���壬������ˮ��������Ӷ���ˮ��
�ʴ�Ϊ���������ƵĻ�ԭ����Fe3+��ˮ������Fe��OH��3���壬������ˮ��������Ӷ���ˮ��
��3���ٶ������ȵķе�ͣ�BΪClO2������װ�ã�Bװ��Ӧ���䣨��ˮ������װ�ã��ʴ�Ϊ������ˮ��������
��CΪβ������װ�ã���ѡ��NaOH��Һ������β��������������ԭ��ӦΪ2ClO2+2NaOH�TNaClO2+NaClO3+H2O��
�ʴ�Ϊ��2ClO2+2NaOH�TNaClO2+NaClO3+H2O��
��4����Na2O2Ͷ��AlCl3��Һ�У������ķ�ӦΪ��2Na2O2+2H2O�T4NaOH+O2���������������Ȼ�������AlCl3+3NaOH=Al��OH��3��+3NaCl������������������������������Һ������������������Ӧ��ʹ�����ܽ⣬��Ӧ�ķ���ʽΪ��Al��OH��3+NaOH=NaAlO2+2H2O��
�ٽ�0.5moLNa2O2Ͷ��lOOmL 3mol/L��ALCL3��Һ�з���������ԭ��Ӧ�ǹ������ƺ�ˮ�����ģ�����ת�����ݴ˷�Ӧ������ϵ���㣬2Na2O2+2H2O�T4NaOH+O2������Ӧ��ÿ��Ӧ2mol�������Ƶ���ת��2mol����0.5moLNa2O2��Ӧ����ת��Ϊ0.5mol��
�ʴ�Ϊ��0.5mol��
��0.5moLNa2O2Ͷ��lOOmL 3mol/LALCL3��Һ�У�2Na2O2+2H2O�T4NaOH+O2����������������1molNaOH��n��Al3+��=0.1L��3mol/L=0.3mol��������ȫ��������Ҫ��������0.9mol��������0.1mol�������ƻ��ܽ�0.1mol������������ƫ�����ƣ�ֱƽ���õ���Ӧ�����ӷ���ʽΪ��10Na2O2+6Al3++6H2O=4Al��OH��3��+2AlO2-+5O2��+20Na+��
�ʴ�Ϊ��10Na2O2+6Al3++6H2O=4Al��OH��3��+2AlO2-+5O2��+20Na+��
���� �������ȼ��仯��������ʿ���������ԭ��Ӧ�����ʵ��Ʊ�ʵ�顢������ԭ��Ӧ����ת�ƺͶ�����ƽ��д���ӷ���ʽ������ϰ���е���Ϣ��֪ʶǨ��Ӧ��Ϊ���Ĺؼ�������ѧ���ۺ�Ӧ����������Ϣ��ȡ�ͷ��������Ŀ��飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
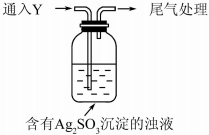 ijѧ����Na2SO3��AgNO3�ڲ�ͬpH�µķ�Ӧ����̽����
ijѧ����Na2SO3��AgNO3�ڲ�ͬpH�µķ�Ӧ����̽����| ʵ�� | pH | ���� |
| A | 10 | ������ɫ�������Ժ��ܽ⣬��Һ���� |
| B | 6 | ������ɫ������һ��ʱ�����δ�ܽ� |
| C | 2 | ����������ɫ������һ��ʱ���������״�غ�ɫ����X |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
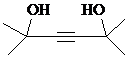 ��
��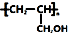 ��д���ϳ�����ͼ�����Լ����ã����ϳ�����ͼʾ�����£�CH2=CH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH��
��д���ϳ�����ͼ�����Լ����ã����ϳ�����ͼʾ�����£�CH2=CH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=5��NH4Cl��Һ�������Һ�У���ˮ������� c��H+����Ϊ10-9mol•L-1 | |
| B�� | �����£���pH=3�Ĵ����pH=11��NaOH��Һ�������Ϻ�pH��7 | |
| C�� | ��c��H+����c��OH-��=1��l012����Һ�У�Na+��I-��NO3-��SO42-�ܴ������� | |
| D�� | 0.1 mol•L-1 Na2CO3��Һ��0.1 mol•L-1 NaHSO4��Һ�������ϣ���Һ�У�c��Na+��+c��H+��=c��CO32-��+c��SO42-��+c��HCO3-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
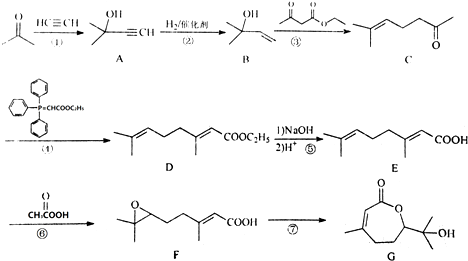
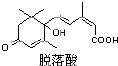 ��������һ������������ֲ�D�أ����ܴ�ʹҶ���������������ṹ��ͼ��ʾ�����й��������˵����ȷ���� ��������
��������һ������������ֲ�D�أ����ܴ�ʹҶ���������������ṹ��ͼ��ʾ�����й��������˵����ȷ���� ��������| A�� | ������Ļ�ѧʽC15H18O4 | |
| B�� | ������ֻ�ܺʹ����������Ӧ | |
| C�� | 1 mol �����������Ժ�2 mol �����Ʒ�����Ӧ | |
| D�� | 1 mol �����������Ժ�2 mol ���������ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | D�Ƿǽ�������ǿ��Ԫ�� | |
| B�� | B�ĵ����ж���ͬ���칹�壬����һ������Ȼ�������Ӳ������ | |
| C�� | B���⻯����ȶ��Դ���D���⻯�� | |
| D�� | A��Cֻ�ܹ��γ����ֻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
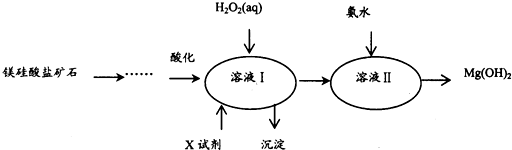
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| ��ʼ����ʱ | 1.5 | 3.3 | 6.5 | 9.4 |
| ������ȫʱ | 3.7 | 5.2 | 9.7 | 12.4 |
 ��
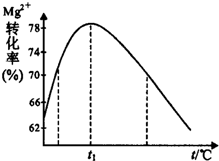
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
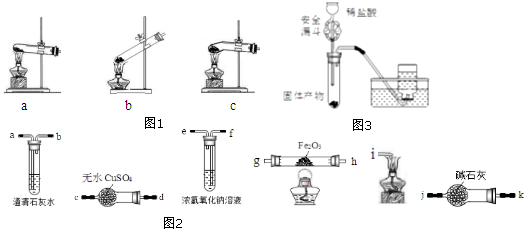
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com