
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的 金属,相关物质间的关系如下图所示。
金属,相关物质间的关系如下图所示。
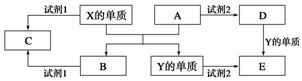
(1)X的单质与A反应的化学方程式是_______________________________________。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是 ________________________________________________________________
________________________________________________________________ ________。
________。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是_____________________________________
________________________________________________________________________。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)________________________________________________________________________。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是________________________________________________________________________。
答案 (1)Fe2O3+2Al Al2O3+2Fe
Al2O3+2Fe
(2)2Al+6H2O+2OH-===2[Al(OH)4]-+3H2↑
(3)①取少量溶液于试管中,滴加几滴KSCN溶液,溶液变血红色,则证明原溶液中含有Fe3+
②Al3++3H2OAl(OH)3+3H+
③2FeSO4+2NaNO2+H2SO4===2Fe(OH)SO4+Na2SO4+2NO↑
解析 (1)X、Y是生活中常见的金属单质,X和A生成Y和B为金属和氧化物反应生成另一种金属和另一种 氧化物,则该反应为铝热反应:Fe2O3+2Al
氧化物,则该反应为铝热反应:Fe2O3+2Al Al2O3+2Fe。(2)若试剂1是NaOH溶液,则该反应为Al和NaOH溶液的反应。(3)若试剂1和试剂2均
Al2O3+2Fe。(2)若试剂1是NaOH溶液,则该反应为Al和NaOH溶液的反应。(3)若试剂1和试剂2均 是稀硫酸,则D为Fe
是稀硫酸,则D为Fe 2(SO4)3,C为Al2(SO4)3。①检验Fe3+利用KSCN溶液。②Al2(SO4)3溶液由于Al3+水解呈酸性。③根据得失电子守恒和质量守恒写出并配平化学方程式。
2(SO4)3,C为Al2(SO4)3。①检验Fe3+利用KSCN溶液。②Al2(SO4)3溶液由于Al3+水解呈酸性。③根据得失电子守恒和质量守恒写出并配平化学方程式。


科目:高中化学 来源: 题型:
某研究性学习小组同学设计如下图所示装置探究氨气的还原性。

(1)氨催化氧化的化学方程式为_____________________________________________
________________________________________________________________________。
(2)若实验时通入氨气的速率过快,在烧瓶中会出现白烟,该物质的化学式为__________。
(3)该小组同学以氨气和二氧化碳为原料制备碳酸氢铵。甲同学先将二氧化碳通入水中,充分溶解后,再通入氨气;乙同学先将氨气通入水中,充分溶解后,再通入二氧化碳。请选择合适的方案并说明原因。
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示。

下列分析错误的是( )
A.AB段的反应为:Fe+2Fe3+===3Fe2+
B.第二份溶液中最终溶质为FeSO4
C.混合酸中NO 物质的量为0.4 mol
物质的量为0.4 mol
D.混合酸中H2SO4浓度为5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学—选修3物质结构与性质](15分)
X、Y、Z、W、R、T为前四周期元素且原子序数依次增大。T原子序数等于X、Y、R原子序数之和。Z为地壳中含量最多的元素。X、Z原子核外均有2个未成对电子。Z与R位于同一主族。X、Y、Z、W、R、T中只有两种金属元素,且存在下列反应:
2W+XZ2  X+2WZ
X+2WZ
回答下列问题:
(1)X、Y、Z的第一电离能最大的是 (用元素符号表示)。
(2)在元素R和元素Z形成的常见化合物中,属于非极性分子的是 (填化学式),该分子中中心原子以 杂化。
(3)由X、T元素组成的单质中一定不存在 (填序号)。
A、离子晶体 B、分子晶体 C、原子晶体 D、金属晶体
(4)基态T原子的核外电子排布式为 。
(5)T+能与NH3通过配位键结合为[T(NH3)n]+。该离子中T+的4s轨道及4p轨道通过sp杂化接受NH3提供的孤电子对。
① [T(NH3)n]+中n= 。
② [T(NH3)n]+中T+与n个氮原子构成的空间结构呈 型。
 (6)化合物WZ和NaCl的晶胞结构形似
(6)化合物WZ和NaCl的晶胞结构形似
(氯化钠晶胞结构如右图所示)。
①在WZ中,阳离子和阴离
子的配位数均为 。
②已知WZ的密度为a g/cm3,
则WZ中距离最近的阳离子间的距离为
pm(用含a的算式表示,阿伏伽德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关物质存在如图所示的转化关系(部分产物已略去)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。

请回答下列问题:
(1)反应①的化学方程式为_________________________________________________
________________________________________________________________________。
(2)反应②的离子方程式为__________________________________________________
[
________________________________________________________________________。
(3)写出另外一种实验室制取H的化学方程式:_______________________________
________________________________________________________________________。
(4)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。将等体积的D溶液与Pb(NO3)2溶液混合,若D的浓度为1×10-2 m ol·L-1,则生成沉淀所需Pb(NO3)2溶液的最
ol·L-1,则生成沉淀所需Pb(NO3)2溶液的最 小浓度为______________。
小浓度为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下有①0.112 L水 ②0.5NA个HCl分子
③25.6 g SO2气体 ④0.2 mol氨气 ⑤2 mol氦气 ⑥6.02×1023个白磷分子,所含原子个数从大到小的顺序为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某气体的摩尔质量为M g·mol-1,NA表示阿伏加德罗常数的值,在一定的温度和压强下,体积为V L的该气体所含有的分子数为X。则 表示的是 ( )
表示的是 ( )
A.V L该气体的质量(以g为单位)
B.1 L该气体的质量(以g为单位)
C.1 mol该气体的体积(以L为单位)
D.1 L该气体中所含的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数的值。下列有关叙述正确的是 ( )
A.分子数为NA的CO、C2H4混合气体的体积约为22.4 L,质量为28 g
B.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中NH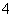 和NO
和NO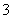 的总数为0.2NA
的总数为0.2NA
C.标准状况下,4.48 L重水(D2O)中含有的中子数为2NA
D.1 mol甲基(—CH3)所含的电子数为9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物在反应中,常有下列原子间的共价键全部或部分断裂如C—H、C—C、C=C、C—O、C═O等。下列各反应中,反应物分子中断裂键的排列,正确的组合是
| 化学反应 | 乙醇酯化 | 乙醇氧化 | 乙醛氧化 | 油脂皂化 | 多肽水解 |
| A | O—H | C—H | C—H | C—O | C—N |
| B | O—H | O—H | O—H | C—O | C—H |
| C | C—O | C—O | C—H | C═O | C═O |
| D | C—O | C—H | C—C | C—O | N—H |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com