
分析 (1)FeCl3溶液与铜反应的实质是三价铁离子与铜反应生成亚铁离子和铜离子;
(2)根据Fe3+、Cu2+的氧化性强弱判断反应先后顺序,从而确定固体的成分、溶液的成分;若固体只有铜,则反应后的溶液中一定无Fe3+存在,一定存在Fe2+,可能含有Cu2+;若有铁剩余,一定有铜生成,Fe3+、Cu2+无剩余,据此进行判断;二价铁离子具有较强的还原性,检验时用氧化剂与其发生氧化还原反应,并且要现象明显,可用紫色的酸性高锰酸钾溶液进行检验.
解答 解:(1)FeCl3溶液与铜反应生成氯化铜和氯化亚铁,反应实质是三价铁离子与铜反应生成亚铁离子和铜离子,反应离子方程式为:2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)由于氧化性:Fe3+>Cu2+,所以向含有氯化铁、氯化铜的溶液中加入一定量的铁粉,反应的反应方程式为:2FeCl3+Fe=3FeCl2、CuCl2+Fe=Cu+FeCl2,若铁过量,一定有铜生成,所以不溶物有铁时,必有铜,a不可能;铁少量时,不溶物只有铜;由于Fe3+能氧化Fe、Cu,充分反应后滤去固体物质,固体为Cu或Fe、Cu,所以滤液中一定无Fe3+,可排除d,固体物质存在两种可能:
①当固体为铜时,溶液中一定无Fe3+,这时可分两种情况:当Cu2+恰好全部参加反应时,溶液中只有Fe2+,故b正确;当Cu2+部分反应生成Fe2+和Cu,所以溶液中还剩有Cu2+,故c正确;
②当固体为铁、铜时,溶液中的Fe3+、Cu2+全部参加反应生成Fe2+和Cu,反应的反应方程式为:2FeCl3+Fe=3FeCl2、CuCl2+Fe=Cu+FeCl2,所以溶液中一定没有Fe3+、Cu2+,一定含有Fe2+,故e正确;
二价铁的检验可用酸性高锰酸钾,若酸性高锰酸钾褪色,说明溶液中含有二价铁,发生反应的离子方程式为:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O,
故答案为:bce;D;MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O.
点评 本题考查金属及其化合物的性质,侧重于学生的分析能力以及元素化合物知识的综合理解和运用的考查,注意把握三价铁离子与铜离子的氧化性强弱,难度不大,掌握元素化合物的性质是关键.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学试卷(解析版) 题型:选择题
某课外活动小组,将剪下的一块镀锌铁片放入试剂瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞溶液,按如图装置进行实验,数分钟后观察,下列现象不可能出现的是
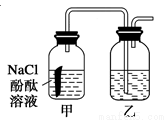
A.乙中导气管中产生气泡
B.乙中导气管里形成一段水柱
C.金属片剪口处溶液变红
D.锌被腐蚀
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高一上10月月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐
B.把燃着的木条插入某瓶无色气体中,木条熄灭,证明瓶中的气体是二氧化碳
C.取少量溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,证明该溶液中一定有硫酸根离子
D.不用任何试剂就可以把KOH、HN03、CuSO4、MgCl2四种溶液鉴别出来
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气是氧化产物 | |
| B. | 还原剂与氧化剂的物质的量之比为1:4 | |
| C. | 若生成4.48 L HF,则转移0.8 mol电子 | |
| D. | O2F2既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
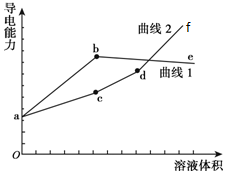 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )| A. | 曲线1代表滴加NaOH溶液的变化曲线 | |
| B. | C点溶液中大量存在的离子是Na+和SO42- | |
| C. | b和d点对应的溶液均显酸性 | |
| D. | be段导电能力下降的原因是NH3•H2O?NH4++OH-,导致离子数目减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高一上10月月考化学试卷(解析版) 题型:选择题
A实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
B在气体发生装置上直接点燃一氧化碳气体时,必须要先检验一氧化碳气体的纯度.最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声
C 制氧气时排水法收集氧气后出现倒吸现象,应立即松开试管上的橡皮塞
D凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com