
| A. | 22 g 2H218O中含有的质子数为10NA | |
| B. | 标准状况下,2.24 L乙醇中含有的C-H键数目为0.5NA | |
| C. | 0.1 mol/L的NaF溶液中所含F-的数目小于0.1NA | |
| D. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去0.5NA个电子 |
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向100mL0.1mol•L-1的Na2CO3溶液中滴加含0.01molCH3COOH的醋酸溶液CO32-+CH3COOH═HCO3-+CH3COO- | |
| B. | 4mol•L-1的NaAlO2溶液和7mol•L-1的盐酸等体积均匀混合4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ | |
| C. | 等物质的量的FeBr2与Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 将少量SO2通入NaClO溶液中:SO2+ClO-+H2O═SO42-+Cl-+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,8g甲烷中含C-H键的数目为4NA | |
| B. | 25℃时,1L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 1 mol冰醋酸和1mol乙醇经催化加热反应生成H2O的分子数为NA | |
| D. | 标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
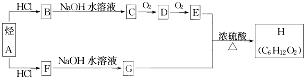
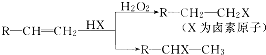
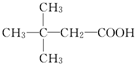 .(用结构简式表示)
.(用结构简式表示)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于相同浓度的弱酸HX和HY(前者的Ka较小)溶液,加水稀释相同倍数时,HY溶液的pH改变值大于HX溶液的pH改变值 | |
| B. | 在NH3•H2O和NH4Cl浓度均为0.1 mol•L-1的体系中,外加少量酸或碱时,溶液的pH可保持基本不变 | |
| C. | 在NaH2PO4水溶液中存在关系:c(H3PO4)+c(H+)=c(HPO42-)+c(PO43-)+c(OH-) | |
| D. | 沉淀溶解平衡AgI?Ag++I- 的平衡常数为8.5×10-17,不能说明难溶盐AgI是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海水中提取镁 | B. | 用酒精测试仪检测酒驾 | ||
| C. | 将氯气通入冷的消石灰中制漂白粉 | D. | 石油分馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
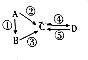
| 物质 | A | B | C | D |
| 元素种类 | 1 | 2 | 3 | 3 |
 ,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 改变压强不一定能改变有气体参与反应的速率 | |
| B. | 增大浓度能加快化学反应速率,原因是增大浓度增加了反应体系中活化分子的百分数 | |
| C. | 温度升高使化学反应速率加快的主要原因是增加了单位体积内活化分子总数 | |
| D. | 催化剂能加快化学反应速率主要原因是降低反应所需的能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com