完成下列各题:
(1)K
2Cr
2O
7(橙色)、Cr
2(SO
4)
3(绿色)、K
2SO
4、H
2SO
4、C
2H
5OH、CH
3COOH和H
2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车.
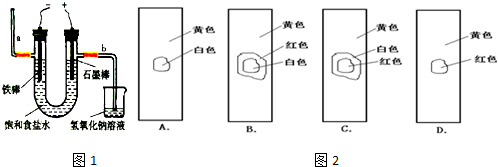
①若司机酒后开车,检测仪器内物质显示出
绿色
绿色
色.
②写出并配平该反应的化学方程式:
2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O
2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O
.
③如果在反应中生成1mol氧化产物,转移的电子总数为
2.408×1024或4NA
2.408×1024或4NA
.
(2)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NO
x、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染.
已知:N
2(g)+O
2(g)=2NO(g)△H=+180.5kJ/mol
2C(s)+O
2(g)=2CO(g)△H=-221.0kJ/mol
C(s)+O
2(g)=CO
2(g)△H=-393.5kJ/mol
①尾气转化的反应之一:2NO(g)+2CO(g)=N
2(g)+2CO
2(g)△H=
-746.5kJ/mol
-746.5kJ/mol
.
②为了提高尾气转化的反应的速率和NO的转化率,采取的正确措施为
B
B
.
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N
2 D.降低温度同时增大压强
③该反应达到平衡时若增大压强,则混合气体的平均相对分子质量
增大
增大
,若升高温度,则该反应的平衡常数
减小
减小
(均填“增大”、“减小”或“不变”).
(3)已知NH
4A溶液为中性,又知将HA溶液加到Na
2CO
3溶液中有气体放出,试推断:
①(NH
4)
2CO
3溶液的pH
>
>
7(填<、>、=).
②相同温度下,等物质的量浓度的下列四种盐溶液按pH由大到小的排列顺序为
c>a>b>d
c>a>b>d
.(填序号)
a.NH
4HCO
3 b.NH
4A c.(NH
4)
2CO
3 d.NH
4Cl.

 名校课堂系列答案
名校课堂系列答案