
下列溶液中有关物质的量浓度关系正确的是:( )
A.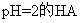 溶液与
溶液与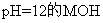 溶液等体积混合:
溶液等体积混合: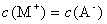
B.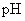 相等的
相等的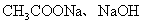 和
和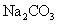 三种溶液:
三种溶液:

C.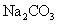 溶液中
溶液中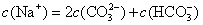
D.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO—) +2c(OH—) = 2c(H+) + c(CH3COOH)
科目:高中化学 来源: 题型:
碱性电池具有容量大、放电电流大的特点,因此得到 广泛的应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应为Zn(s)+2MnO2(s)+H2O== Zn(OH)2(s)+ Mn2O3(s),下列说法错误的是
A. 电池工作时,锌失去电子
B. 电池负极的电极反应式为:Zn-2e-+2OH-== Zn(OH)2
C. 电池工作时,电子由正极通外电路流向负极
D. 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是:( )
A.金属铝溶于氢氧化钠溶液: 2Al + 6OH- = 2AlO2- + 3H2↑
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ═ Al(OH)3↓
C.用FeCl3溶液腐蚀铜电路板: Fe3++ Cu = Fe2++ Cu2+
D.铜片加入浓硝酸中:Cu+4H++2NO3-=Cu2++2H2O+2NO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在固定容积的密闭容器中,能表示反应X(g)+2Y(g)  2Z(g)一定达到化学平衡状态的是:
2Z(g)一定达到化学平衡状态的是:
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中气体的压强不再发生变化
④单位时间内生成n mol Z,同时生成n mol X
A.①② B.①④
C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃、101kPa下,如右图所示,石墨的燃烧热为393.5kJ/mol,金刚石的燃烧热为395.0kJ/mol 。下列说法或表达正确的是:
A.金刚石比石墨稳定
B.C(s、石墨)=C(s、金刚石) △H =+1.5kJ/mol
C.△H1<△H2
D.如果使用催化剂,△H1和△H2都变小

查看答案和解析>>
科目:高中化学 来源: 题型:
下列化合物:①HCl ②NaOH ③CH3COOH ④NH3·H2O ⑤CH3COONa ⑥NH4Cl ⑦C2H5OH ⑧SO2
(1)属于弱电解质的是 ,溶液呈碱性的有 (填序号)。
(2)常温下0.01 mol/L NaOH溶液的pH= ;pH=11的CH3COONa溶液中由水电离产生的c(OH-) = 。
mol/L NaOH溶液的pH= ;pH=11的CH3COONa溶液中由水电离产生的c(OH-) = 。
(3)用离子方程式表示CH3COONa溶液呈碱性的原因 ,其溶液中离子浓度按由大到小的顺序为 。
 (4)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
(4)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
①由图中信息可知HA为_______酸
(填“强”或“弱”)。
②在滴加过程中,水的电离程度的变化是先 后 (填“增大”、“减小”或“不变”)
③K点对应的溶液中, c(M+)+c(MOH)= mol·L-1。
(5)在25 ℃下,向浓度均为0.01 mol·L-1的FeCl3和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),当测得溶液pH=11时,则此温度下残留在溶液中的c(Cu2+):c(Fe3+)
= 。
(已知25℃时Ksp[Fe(OH)3]=4.0×10-38, Ksp[Cu(OH)2]=2.2×10-20)
(6)25℃时,将bmol NH4NO3溶于水,向该溶液滴加aL氨水后溶液呈中性,则所滴加氨水的浓度为_______mol·L-1。(NH3·H2O的电离平衡常数取Kb = 2×10-5 mol·L-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.Al、Fe、Cu三者对应的氧化物均为碱性氧化物
B.向污水中投放明矾,能生成凝聚悬浮物的Al(OH)3胶体,起到净水的作用
C.向NaAlO2溶液中通入过量CO2:2AlO +CO2+3H2O===2Al(OH)3↓+CO
+CO2+3H2O===2Al(OH)3↓+CO
D.加入铝粉能产生H2的溶液中,一定存在大量的Na+、Ba2+、AlO 、Cl
、Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
2009年4月22日是第40个世界地球日,今年世界地球日的主题是“绿色世纪”。下列行为不符合这一主题的是
A.分类回收、利用垃圾,减少资源浪费
B.推广使用一次性木筷,减少疾病传染
C.开发风能等洁净能源,减少使用化石燃料
D.研究煤和石油脱硫新技术,减少酸雨发生
查看答案和解析>>
科目:高中化学 来源: 题型:
铝热反应常用于冶炼高熔点的金属, 可简单认为是铝与某些金属氧化物在高温条件下发生的反应。某学习小组对铝热反应(以Al和Fe2O3反应为例)实验进行研究。
查阅数据得到Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下表所示:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1565 |
| 沸点/℃ | 2467 | 2980 | 2750 | ┄ |
试回答下列问题:
(1)在铝热反应中金属铝表现出 性(填“氧化”或“还原”)。请判断下列金属中那一个不能由铝热反应制取 。(填序号)
①Fe ②Cr(铬) ③V(钒) ④Ca ⑤Mn
(2)某同学推测,铝热反应所得到的熔融物中应含有铁、铝两种金属。如设计一个简单的实验方案证明该熔融物中含有金属铝,则实验所需用的试剂为 ,可观察到的实验现象是 。
(3)另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物投入到少量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色未变血红色,即可证明熔融物中不含有Fe2O3。则
①物质甲是 (填化学式)。
②该同学的实验方案是否合理? (填“合理”或“不合理”)。
理由:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com