
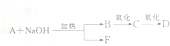
分析 A具有香味的有机物,A水解生成具有相同碳原子的酸和醇,则A为酯,在碱性条件下水解得B和F,B能两步氧化,则B为醇,C为醛,D为羧酸,0.6g D物质可以配成0.2mol/L,D溶液50mL,则D的相对分子质量为$\frac{0.6}{0.2×0.05}$=60,则D为CH3COOH,所以B为CH3CH2OH,C为CH3CHO,D与氢氧化钠溶液反应可生成F为CH3COONa,故A为CH3COOCH2CH3,据此答题.
解答 解:A具有香味的有机物,A水解生成具有相同碳原子的酸和醇,则A为酯,在碱性条件下水解得B和F,B能两步氧化,则B为醇,C为醛,D为羧酸,0.6g D物质可以配成0.2mol/L,D溶液50mL,则D的相对分子质量为$\frac{0.6}{0.2×0.05}$=60,则D为CH3COOH,所以B为CH3CH2OH,C为CH3CHO,D与氢氧化钠溶液反应可生成F为CH3COONa,故A为CH3COOCH2CH3,
(1)根据上面的分析可知,A为CH3COOCH2CH3,A的名称为乙酸乙酯,故答案为:乙酸乙酯;
(2)B→C的化学方程式为2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O;
(3)根据上面的分析可知,D的结构简式为CH3COOH,故答案为:CH3COOH;
(4)B为CH3CH2OH,比B少一个碳原子的同系物的结构简式为CH3OH,故答案为:CH3OH.
点评 本题主要考查了有机物之间的相互转化关系,难度不大,答题是要熟练掌握常见官能团之间的相互转化关系,灵活运用基础知识分析问题.


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:选择题
| A. | 12g金刚石晶体中含有的C-C的数目为2NA | |
| B. | 1L1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| C. | 5.6gFe与足量的水蒸气完全反应,转移电子的数目为0.2NA | |
| D. | 标准状况下,22gCO2气体中含有的σ键和π键的数目均为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
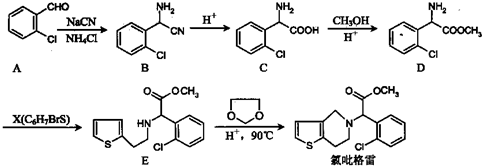
 .
. .
.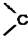 =O$→_{H+}^{ROH}$
=O$→_{H+}^{ROH}$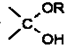 $→_{H+}^{ROH}$
$→_{H+}^{ROH}$ 写出由乙烯、甲醇为有机原料制备化合物
写出由乙烯、甲醇为有机原料制备化合物 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2$\stackrel{Br_{2}}{→}$CH2Br•CH2Br.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2$\stackrel{Br_{2}}{→}$CH2Br•CH2Br.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
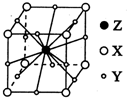 X、Y、Z、W为短周期元素且原子序数依次增大.X的一种气态氢化物m可用来焊接或切割金属,且该分子所有原子在一条直线上.Y2-的M能层的原子轨道为全空状态.Z的单质用作铝热反应的引燃剂. W与X形成的化合物是一种常见的有机溶剂n.A为第四周期元素,其基态原子含有6个未成对电子.
X、Y、Z、W为短周期元素且原子序数依次增大.X的一种气态氢化物m可用来焊接或切割金属,且该分子所有原子在一条直线上.Y2-的M能层的原子轨道为全空状态.Z的单质用作铝热反应的引燃剂. W与X形成的化合物是一种常见的有机溶剂n.A为第四周期元素,其基态原子含有6个未成对电子.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 7:2 | B. | 4:5 | C. | 5:4 | D. | 2:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去MgCl2溶液中的Fe3+,可向溶液中加入氨水调节pH | |
| B. | 除去污水中的金属离子Cu2+、Hg2+,可向溶液中加入FeS | |
| C. | 除去Cl2中混有的HCl,可以将气体通入饱和氯化钠溶液 | |
| D. | 除去CaCO3中的少量CaSO4,可以向其中加入足量饱和Na2CO3溶液后过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H、N、Na、Fe、V五种元素中,有两种是第四周期元素 | |
| B. | 铁元素位于周期表中的第四周期,第8纵行,属于第ⅧA族 | |
| C. | 第四、五、六、七周期,每周期的元素共有18种 | |
| D. | 碱金属元素是指第ⅠA族的所有元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com