
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料.实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)212H2O]的工艺流程如图所示: 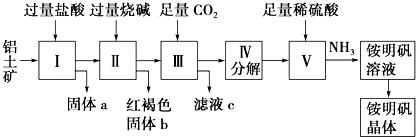 请回答下列问题:
请回答下列问题:
(1)固体a的化学式为 , Ⅲ中通入足量CO2气体发生反应的离子方程式为 .
(2)由Ⅴ 制取铵明矾溶液的化学方程式为 . 从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)、冷却结晶、过滤洗涤.
(3)以1000kg含氧化铝36%的铝土矿为原料制取Al2(SO4)3 , 需消耗质量分数98%的硫酸(密度1.84gcm﹣1)L(计算结果请保留一位小数).
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量.若欲使制得的铵明矾和硫酸铝的物质的量之比为1:1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为 .
【答案】
(1)SiO2;AlO2﹣+CO2+2H2O═HCO3﹣+Al(OH)3↓
(2)Al2O3+4H2SO4+2NH3═2NH4Al(SO4)2+3H2O;蒸发浓缩
(3)575.4
(4)3:10
【解析】解:(1)铝土矿中Al2O3和Fe2O3能溶于盐酸,SiO2不溶于盐酸,所以固体a的化学式为SiO2 , Al2O3溶于烧碱生成NaAlO2溶液,在其中通入CO2生成Al(OH)3沉淀,所以答案是:SiO2; AlO2﹣+CO2+2H2O═HCO3﹣+Al(OH)3↓;(2)Al(OH)3分解生成Al2O3 , Al2O3与稀硫酸、氨气反应生成铵明矾溶液,从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、过滤洗涤,所以答案是:Al2O3+4H2SO4+2NH3═2NH4Al(SO4)2+3H2O;蒸发浓缩;(3)m(Al2O3)=1 000 kg×36%=360 kg, 依据:
Al2O3+ | 3H2SO4=Al2(SO4)3+3H2O |
102 | 294 |
360kg | m(H2SO4) |
故m(H2SO4)= ![]() =1037.6 kg,需消耗质量分数98%的硫酸(密度1.84 gcm﹣3)为=
=1037.6 kg,需消耗质量分数98%的硫酸(密度1.84 gcm﹣3)为= ![]() =575.4 L,
=575.4 L,
所以答案是:575.4;(4)设制得的Al2(SO4)3和NH4Al(SO4)212H2O的物质的量都是1 mol,则Al3+共3 mol,SO42﹣共5 mol,根据Al3+和SO42﹣守恒原理可得,加入Al2O3和H2SO4的物质的量之比为: ![]() :5=3:10,所以答案是:3:10.
:5=3:10,所以答案是:3:10.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )。
A. 硅胶常用于作干燥剂 B. 氢氟酸可以用来刻蚀玻璃
C. 硅的化学性质很稳定,主要以游离态存在于自然界 D. 硅酸钠的水溶液俗称水玻璃,可用于制备木材防火剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分.
碳 | 氮 | Y | |
X | 硫 | Z |
请判断 X、Y、Z,并用相应的元素符号回答下列问题.
(1)X是 , 它的原子M层电子数是 .
(2)表中元素原子半径最大的是 .
(3)Y在元素周期表中的位置是第周期第族,用电子式表示Y的最简单氢化物的形成过程 .
(4)氮气中氮原子之间的化学键属于键,由氮气与氢气反应生成1mol氨气时转移电子的数目是NA .
(5)硫与Z两种元素相比,非金属性强的是 , 请用化学方程式说明这一结论 .
(6)碳、氮、Y三种元素的最简单气态氢化物的稳定性由强到弱的顺序是 . 由最高价碳元素与最低价氮元素组成化合物的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气中的氮氧化物(NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气污染.在25℃,101kPa下,1molO3与烟气中的NO完全反应生成NO2 , 同时放热317.3kJ.请计算:
(1)标准状况下,1m3烟气中含NO 0.224L,要处理3m3烟气中的NO,需O3的体积.
(2)上述 O3与NO在25℃,101kPa下,完全反应时产生的热量.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X+Y═M+N反应中的能量变化过程如图,则下列有关说法正确的是( ) 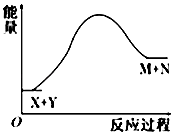
A.X的能量一定低于M的能量,Y的能量一定低于N的能量
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习要建构若干基本观念,以下四类化学基本观念中认识不正确的是( )
A. 元素观:金刚石和石墨均由碳元素组成
B. 分类观:从组成上看干冰和酒精都属于氧化物
C. 变化观:氢气和水可以相互转化
D. 微粒观:一个一氧化碳分子由一个碳原子和一个氧原子构成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g) ![]() CH3OCH3(g)
CH3OCH3(g)
+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡。该反应中CO2的平衡转化率随温度的变化曲线如图所示。下列说法正确的是

A.反应2CO2(g)+6H2(g) ![]() CH3OCH3(g) + 3H2O(g)的 △S<0、△H<0
CH3OCH3(g) + 3H2O(g)的 △S<0、△H<0
B.表示乙容器CO2的平衡转化率随温度变化的是曲线B
C.体系中c(CH3OCH3):c(CH3OCH3,状态Ⅱ)<2c(CH3OCH3,状态Ⅲ)
D.逆反应速率v逆:v逆(状态Ⅰ)<v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容密闭容器中,不是可逆反应A(g)+3B(g)![]() C(g)达到平衡标志的是( )
C(g)达到平衡标志的是( )
A. 3v正(A)=v逆(B) B. 单位时间内生成a molA,同时生成3a molB
C. A、B、C的浓度不再变化 D. 容器内的总压强不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com