
| A、①②③⑥ | B、①②④ |
| C、③⑤⑥ | D、③⑤ |


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:
| A、汽油、柴油和植物油都是碳氢化合物 |
B、β-月桂烯的结构如图 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
| C、植物油通过加氢可以变为脂肪 |
| D、煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏制取 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、-488.3 kJ/mol |
| B、-244.15 kJ/mol |
| C、+488.3 kJ/mol |
| D、+244.15 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Cu2(OH)2CO3
| ||||
B、Ca(HCO3)2
| ||||
C、2KClO3
| ||||
D、3Fe+4H2O(g)
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在强碱溶液中次氯酸钠与Fe(0H)3反应生成Na2FeO4:3ClO-+2Fe(0H)3=2FeO42-+3Cl-+H2O+4H+ |
| B、从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| C、以金属银为阳极电解饱和硫酸铜溶液:Cu2++2 H2O=2Cu+O2 ↑+4H+ |
| D、过氧化氢能使酸性KMnO4溶液褪色:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,PH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B、标准状况下,11.2L的戊烷所含的分子数为0.5NA |
| C、标准状况下,2.24 L Cl2溶于水中达到饱和,转移的电子数是0.1NA |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
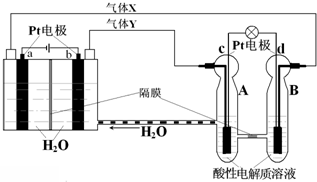 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )| A、转移0.1mol电子时,a电极产生1.12LH2(标准状况) |
| B、b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH- |
| C、c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池 |
| D、d电极上发生的电极反应是:O2+4H++4e-=2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com