
| A. | 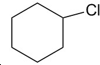 | B. | 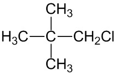 | C. | 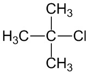 | D. | 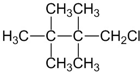 |
分析 A、环己烷中只存在1种化学环境不同的H,此卤代烃可以由环己烷取代得到;
B、2,2-二甲基丙烷只存在一种H,此有机物可以由2,2-二甲基丙烷取代得到;
C、2-甲基丙烷中存在2种化学环境不同的H,一氯代物存在同分异构体;
D、2,2,3,3-四甲基丁烷中只存在一种环境的H,一氯代物只有一种,据此解答即可.
解答 解:A、 可以由环己烷取代制得,故A不选;
可以由环己烷取代制得,故A不选;
B、 可以由2,2-二甲基丙烷取代得到,故B不选;
可以由2,2-二甲基丙烷取代得到,故B不选;
C、2-甲基丙烷中存在2种化学环境不同的H,一氯代物存在同分异构体,故 不适合由相应的烃经卤代反应制得,故C选;
不适合由相应的烃经卤代反应制得,故C选;
D、 可以由2,2,3,3-四甲基丁烷制得,故D不选,故选C.
可以由2,2,3,3-四甲基丁烷制得,故D不选,故选C.
点评 本题主要考查的是一氯代物的同分异构体的判断,制取氯代烃的途径和方法必须满足制取的副反应产物最少为好,难度不大.


科目:高中化学 来源: 题型:解答题
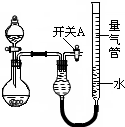 某同学设计如图所示装置分别进行探究实验(夹持装置已略去)
某同学设计如图所示装置分别进行探究实验(夹持装置已略去)| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| ① | Cu、稀HNO3 | H2O | |
| ② | NaOH固体、浓氨水 | NH3 | |
| ③ | Na2CO3固体、稀H2SO4 | CO2 | |
| ④ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
| 编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
| 1 | 1.0g | 10.0mL | 347.5mL |
| 2 | 1.0g | 10.0mL | 335.0mL |
| 3 | 1.0g | 10.0mL | 344.5mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| A | 原子半径是周期表所有元素中最小的 |
| B | 单质常温下为双原子分子,其氢化物水溶液使酚酞变红 |
| C | 基态原子核外S能级上有电子,且p能级上只有一个轨道排满 |
| D | 同周期中电负性最小 |
| E | E的族序数与周期数之差为4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第三次月考模拟化学试卷 题型:选择题
如下图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O。下列说法正确的是

A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化为电能的装置
B.甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+
C.反应一段时间后.向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度
D.甲池中消耗280mL(标准伏况下)O2,此时丙池中理论上最多产生1.45g固体
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第三次月考模拟化学试卷 题型:选择题
向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性。金属离子已完全沉淀.沉淀质量为39.2g.下列有关说法不正确的是
A.Cu与Cu2O的物质的量之比为2:1
B.硝酸的物质的量浓度为2.4mol/L
C.产生的NO在标准状况下的体积为4.48L
D.Cu、Cu2O与硝酸反应后剩余HNO3为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com