
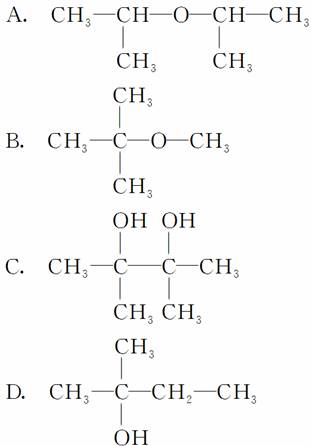
某含氧有机化合物A可以作为无铅汽油的抗爆震剂,它的相对分子质量为88.0,其中含碳元素质量分数为68.2%,含氢元素质量分数为13.6%,经红外光谱和核磁共振氢谱显示该分子中有4个甲基,则A的结构简式为( )
科目:高中化学 来源: 题型:
已知 H2SO4(aq)与 Ba (OH)2(aq)反应的 ΔH=-1 584.2 kJ·mol-1;HCl (aq) 与NaOH (aq) 反应的 ΔH=-55.6 kJ·mol-1。则生成 BaSO4 (s) 的反应热等于 ( )。
A.-1 528.6 kJ·mol-1 B.-1 473 kJ·mol-1
C.+1 473 kJ·mol-1 D.+1 528.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
氮元素的化合物应用十分广泛。请回答:
(1)火箭燃料液态偏二甲肼(C2H8N2)是用液态N2O4作氧化剂,二者反应放出大量的热,生成无毒、无污染的气体和水。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,则该反应的热化学方程式为 。

(2)298 K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g) ΔH=-a kJ/mol (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
N2O4(g) ΔH=-a kJ/mol (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
①298k时,该反应的平衡常数为 L·mol-1(精确到0.01)。
②下列情况不是处于平衡状态的是 :
A.混合气体的密度保持不变; B.混合气体的颜色不再变化; C.气压恒定时
③若反应在398K进行,某时刻测得n(NO2)=0.6 moln(N2O4)=1.2mol,则此时V(正) V(逆)(填 “>”、“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点。
①b点时,溶液中发生水解反应的离子是______;
②在c点,溶液中各离子浓度由大到小的排列顺序 。
③d、e点对应溶液中,水电离程度大小关系是d e(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在可逆反应中,平衡常数与反应进行的限度的关系正确的是( )
A.K越大,反应程度越大
B.K越大,反应程度越小
C.K的大小与反应程度无关
D.升高温度,K增大
查看答案和解析>>
科目:高中化学 来源: 题型:
放热反应CO(g)+H2O(g)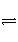
 CO2(g)+H2(g)在温度t1时达到平衡,[CO]1=[H2O]1=1.0 mol·L-1,其平衡常数为K1。其他条件不变,升高反应体系的温度至t2时,反应物的平衡浓度分别为[CO]2和[H2O]2,平衡常数为K2,则( )
CO2(g)+H2(g)在温度t1时达到平衡,[CO]1=[H2O]1=1.0 mol·L-1,其平衡常数为K1。其他条件不变,升高反应体系的温度至t2时,反应物的平衡浓度分别为[CO]2和[H2O]2,平衡常数为K2,则( )
A.若增大CO浓度,K2和K1都增大 B.K2>K1
C.[CO]2=[H2O]2 D.[CO]1>[CO]2
查看答案和解析>>
科目:高中化学 来源: 题型:
某高聚物可表示为
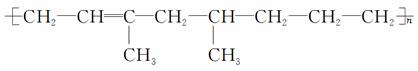
下列有关叙述错误的是( )
A.该高聚物是通过加聚反应生成的
B.合成该高聚物的单体有3种
C.该物质能被酸性KMnO4溶液氧化
D.1 mol该物质与1 mol H2加成,生成不含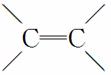 的物质
的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
为测定某有机物A的结构,进行如下实验:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4 g H2O和8.8 g CO2,消耗氧气6.72 L(标准状况下),则该物质中各元素的原子个数比是________。
(2)质谱仪测定有机化合物的相对分子质量为46,则该物质的分子式是________。
(3)根据价键理论,预测A的可能结构并写出结构简式________。
(4)核磁共振氢原子光谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种数和数目,例如:甲基氯甲基醚(Cl—CH2—O—CH3)有两种氢原子,其核磁共振氢谱如图Ⅰ所示,经测定,有机物A的核磁共振氢谱示意图如图Ⅱ所示,则A的结构简式为________。

(5)A在一定条件下脱水可生成B,B可合成包装塑料C,请写出B转化为C的化学反应方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一。下列对有关实验事实的解释正确的是( )
A.SO2气体使高锰酸钾溶液褪色,表现了SO2的漂白性
B.在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是Cu
C.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
D.常温下,将铝片放入浓硫酸中,无明显现象,说明铝不与冷的浓硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
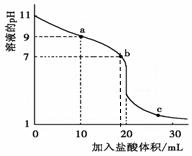
室温下,将0.100 0 mol·L-1盐酸滴入20.00 mL 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如右图。下列有关说法不正确的是
A.该一元碱溶液浓度为0.100 0 mol·L-1
B.a、b、c点的水溶液导电性依次增强
C.室温下,MOH的电离常数Kb=1×10-5
D.b点:c(M+)+c(MOH)=c(Clˉ)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com